La vaina periodontal se refiere al conjunto de tejidos que rodean y envuelven la raíz dentaria, esencialmente el ligamento periodontal y sus estructuras asociadas, formando una envoltura fibrosa que fija el diente al hueso alveolar. En términos anatómicos, equivale a la membrana periodontal o ligamento periodontal, un tejido conectivo especializado que actúa como un estuche vasculonervioso lleno de fibras colágenas, elásticas, vasos sanguíneos y nervios, insertado entre el cemento radicular del diente y el alveolo óseo.
Esta “vaina” fibrosa mantiene suspendido al diente dentro de su alveolo, permitiendo una leve movilidad fisiológica y funcionando como medio de unión y amortiguación. Su importancia en odontología moderna es fundamental: un periodonto sano (incluyendo la vaina periodontal íntegra) garantiza que el diente se mantenga firme pero con capacidad de absorber las fuerzas masticatorias, además de servir como vía de sensibilidad y nutrición. La pérdida o alteración de esta vaina periodontal - como ocurre en la enfermedad periodontal avanzada - conduce a movilidad dentaria y, eventualmente, a la pérdida del diente.
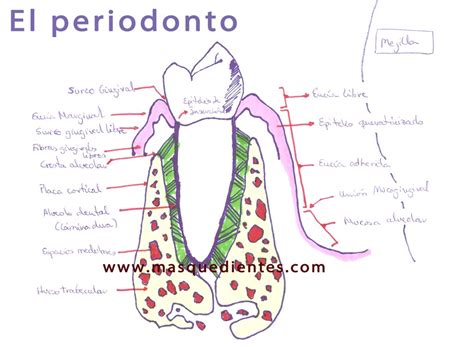
Componentes Principales de la Vaina Periodontal
La vaina periodontal está principalmente conformada por el ligamento periodontal, un tejido conectivo fibroso de espesor variable (aproximadamente 0,2 a 0,5 mm de ancho en condiciones normales) que rodea completamente la raíz dental. Sus componentes principales son haces de fibras colágenas tipo I organizados en grupos específicos con orientaciones definidas, complementados por fibras elásticas (elaunina y oxitalán) y una matriz extracelular rica en proteoglicanos y glicoproteínas.
Las Fibras de Sharpey
Estas fibras colágenas se insertan de un lado en el cemento radicular y del otro en el hueso alveolar, constituyendo las llamadas fibras de Sharpey en sus extremos de anclaje. Gracias a este sistema de fibras, el ligamento periodontal conecta firmemente el diente al alveolo, suspendiéndolo en una suerte de hamaca microscópica dentro del hueso.
Las fibras principales del ligamento se disponen en varios grupos funcionales:
- Grupo crestal (cerca del cuello dental, desde el cemento hacia la cresta ósea)
- Grupo horizontal
- Grupo oblicuo (el más numeroso, orientado en diagonal desde el cemento hacia el hueso, ofreciendo resistencia contra fuerzas verticales)
- Grupo apical (en el vértice de la raíz)
- Interradicular (entre raíces de piezas multirradiculares)
Además de fibras, la vaina periodontal contiene una abundante población celular. Predominan los fibroblastos periodontales, encargados de sintetizar y remodelar las fibras de colágeno; también hay células mesenquimales indiferenciadas (células madre del ligamento periodontal) que pueden transformarse en osteoblastos, cementoblastos u otros tipos celulares según las necesidades de reparación. En la superficie del cemento radicular suelen encontrarse cementoblastos aplanados, mientras que en la cara ósea aparecen osteoblastos y osteoclastos activas durante el remodelado.
Vascularización e Inervación
Un rasgo crucial de la vaina periodontal es su rica vascularización e inervación. El ligamento periodontal está atravesado por capilares sanguíneos provenientes de los vasos alveolares y ramas arteriales de la pulpa, que le aportan nutrientes tanto a él como al cemento y hueso adyacentes. También lo recorren numerosas fibras nerviosas sensitivas (receptoras de presión, tacto fino y dolor) y autónomas simpáticas (que regulan el calibre vascular). Esta provisión vasculonerviosa convierte al periodonto en un tejido altamente dinámico y sensible.
Microscopicamente, el ligamento periodontal es un tejido blando altamente celular y vascularizado, distinto de un ligamento articular típico: presenta uno de los índices de recambio de colágeno más altos del organismo, adaptándose constantemente a los cambios de función mecánica. La unión cemento-hueso alveolar a través de la vaina periodontal constituye una articulación especializada denominada gonfosis.
A diferencia de la unión rígida de un implante dental al hueso, la presencia de esta vaina fibrosa le confiere al diente cierto grado de movilidad elástica y capacidad de amortiguación. El cemento radicular, que carece de vasos y nervios, recibe nutrientes por difusión desde el ligamento periodontal, y sus fibras extrínsecas (de Sharpey) quedan parcial o totalmente mineralizadas al incorporarse en el cemento (especialmente en el cemento acelular del tercio cervical).
Del lado del hueso alveolar, las fibras perforantes se entrelazan con el periostio interno del alveolo y suelen mineralizarse en su periferia, contribuyendo a la continuidad entre el ligamento y el hueso.
Fibras del ligamento periodontal - Periodoncia
Funciones Biológicas Esenciales de la Vaina Periodontal
Funcionalmente, la vaina periodontal desempeña múltiples roles biológicos esenciales: sostén, amortiguación, sensorial, nutritivo y remodelador. Su papel de sostén es obvio: mantiene el diente unido al hueso, resistiendo las fuerzas masticatorias.
Las fibras colágenas oblicuas, al tensarse bajo carga, absorben impactos y evitan que la presión se transmita directamente al hueso alveolar; actúan como un “amortiguador” que disipa las fuerzas durante la masticación. Esta capacidad amortiguadora protege tanto al hueso (evitando microfracturas) como a la dentina/pulpa (evitando traumatismos por golpes).
Desde el punto de vista sensorial, los abundantes mecanorreceptores periodontales proporcionan al sistema nervioso central información preciso-propioceptiva sobre la posición y fuerza ejercida sobre cada diente. Gracias a ello, regulamos inconscientemente la fuerza de mordida y la coordinación masticatoria; por ejemplo, podemos detectar un grano de arena entre los alimentos o alinear los dientes antagonistas en máxima intercuspidación con delicadeza.
Biológicamente, el ligamento periodontal es un tejido en constante renovación y adaptación. Sus fibroblastos sintetizan nuevas fibras colágenas y eliminan las viejas mediante colagenasas, manteniendo un equilibrio según las demandas funcionales. Si un diente deja de ocluir (por ejemplo, la pieza antagonista se pierde), el ligamento periodontal tiende a adelgazarse y las fibras se vuelven más laxas.
Por el contrario, en dientes sometidos a cargas intensas o hábitos parafuncionales, el espacio periodontal puede ensancharse y las fibras refuerzan su inserción, mostrando un patrón estructural más marcado (hiperfunción). Este principio se aprovecha en ortodoncia: al aplicar fuerzas controladas sobre un diente, se crea presión en un lado del ligamento (donde disminuye el flujo sanguíneo y se activan osteoclastos para reabsorber hueso) y tensión en el lado opuesto (donde el estiramiento de las fibras y el aumento de flujo estimulan osteoblastos para formar hueso nuevo). Así, el diente se mueve gradualmente dentro del alveolo mediante un remodelado óseo guiado por los cambios en el ligamento periodontal.
En cuanto a su rol nutritivo, los vasos sanguíneos del ligamento periodontal aseguran la supervivencia de las células del propio ligamento, del cemento adyacente (manteniendo viables a los cementoblastos y cementocitos) y contribuyen a la irrigación periférica de la pulpa en la zona apical. Esta rica irrigación es también parte del motivo de la rápida cicatrización que puede lograr el periodonto bajo condiciones favorables.
Sin embargo, la misma vascularización abundante facilita la propagación de la inflamación en casos de periodontitis: mediadores inflamatorios y células inmunes alcanzan rápidamente todo el ligamento y el hueso alveolar circundante, llevando a la destrucción difusa de las fibras y del soporte óseo si la infección periodontal progresa.
Regeneración Periodontal
La regeneración periodontal es un campo de intensa investigación, con el objetivo de reconstruir la vaina periodontal perdida por enfermedad o trauma. Un avance significativo ha sido el aislamiento de células madre del ligamento periodontal (PDLSCs), las cuales en modelos preclínicos han demostrado capacidad para regenerar cemento y fibras periodontales cuando se siembran en andamios adecuados.
Ensayos experimentales han utilizado láminas celulares (cell sheets) cultivadas de ligamento periodontal que, al aplicarse sobre raíces expuestas, han logrado nuevo anclaje de fibras colágenas funcionales al diente y neoformación de hueso alveolar en defectos críticos. Asimismo, se están desarrollando andamios tridimensionales biofabricados que imitan la inserción periodontal: por ejemplo, membranas de colágeno o scaffolds porosos bifásicos que tienen una cara osteoconductora (para guiar la regeneración del hueso alveolar) y otra superficie cementoconductora (para promover la deposición de cemento y la inserción de fibras del ligamento).

El Cemento Radicular
El cemento radicular es un tejido conectivo calcificado especializado que cubre la dentina de la raíz del diente, desde la unión amelocementaria (línea cervical) hasta el ápice radicular. Presenta una mineralización menor que la del esmalte pero comparable a la de la dentina, y su función primordial es servir de anclaje a las fibras del ligamento periodontal en la superficie de la raíz, asegurando la fijación del diente al hueso alveolar.
Este tejido constituye una parte esencial del periodonto de inserción, actuando como elemento biomecánico clave que permite la unión funcional entre el diente y el hueso maxilar o mandibular. A diferencia del esmalte, el cemento se deposita durante toda la vida del diente, participando en procesos de adaptación y reparación: contribuye a compensar el desgaste oclusal mediante aposición adicional, a adaptarse a cambios en las cargas masticatorias y a proteger la raíz ante lesiones o agresiones patológicas mediante formación de tejido nuevo.
En la odontología moderna, la integridad y potencial de regeneración del cemento radicular revisten gran importancia clínica, ya que este tejido juega un rol crítico en la estabilidad periodontal y en la cicatrización tras enfermedades periodontales.
Composición Química y Estructura del Cemento
El cemento radicular tiene una composición química similar a la de otros tejidos mineralizados, conformada aproximadamente por un 45-50% de matriz inorgánica (principalmente cristales de hidroxiapatita cálcica) y un 50-55% de componente orgánico y agua (predominando colágeno tipo I junto a proteoglicanos y glicoproteínas). Esta proporción mineral le confiere una dureza menor que la dentina y muy inferior a la del esmalte, situando su resistencia en un rango intermedio entre el hueso y la dentina.
Macroscópicamente, el cemento es de color amarillo pálido y, al estar menos mineralizado, resulta más poroso y blando que la dentina; cuando queda expuesto por recesión gingival puede desgastarse con facilidad por abrasión mecánica y ser susceptible a la caries radicular.
Tipos de Cemento Radicular
Existen distintas variantes de cemento radicular definidas por la presencia o ausencia de células y por el origen de sus fibras colágenas. Se distingue principalmente un cemento acelular de fibras extrínsecas (cemento primario) y un cemento celular de fibras mixtas (cemento secundario).
- Cemento acelular de fibras extrínsecas (CAFE): Ubicado en el tercio cervical y medio radicular, constituye el primer cemento formado durante el desarrollo dental. Su matriz presenta abundantes fibras de Sharpey (fibras extrínsecas del ligamento periodontal) que penetran perpendicularmente a la superficie radicular, proporcionando anclaje sólido para la inserción periodontal. Carece de células incluidas y su espesor oscila entre 30-50 μm.
- Cemento celular de fibras mixtas (CCFM): Localizado principalmente en el tercio apical y zonas de furcación radicular, contiene tanto fibras extrínsecas (Sharpey) como intrínsecas (producidas por cementoblastos). Presenta cementocitos atrapados en lagunas dentro de su matriz y su formación continúa a lo largo de la vida.
- Cemento acelular afibrilar (CAA): Representa una delgada capa (1-15 μm) predominantemente mineralizada sin fibras colágenas ni células, que puede encontrarse cubriendo pequeñas áreas del esmalte cervical o como parches sobre la superficie radicular.
- Cemento celular de fibras intrínsecas (CCFI): Formado exclusivamente por fibras producidas por cementoblastos (sin fibras de Sharpey), aparece principalmente como tejido reparativo tras reabsorciones radiculares o traumatismos.
Cementogénesis
El cemento radicular se forma durante el desarrollo de la raíz dental mediante el proceso de cementogénesis. Una vez que la vaina epitelial de Hertwig ha estimulado la diferenciación de odontoblastos radiculares y se ha depositado la primera capa de dentina radicular, dicha vaina epitelial se fragmenta y permite que células ectomesenquimáticas del folículo dental accedan a la superficie de la dentina recién formada.
Bajo la influencia de factores de crecimiento y señales moleculares específicas, estas células del folículo se diferencian en cementoblastos, los cuales se disponen sobre la dentina radicular y comienzan a depositar una matriz orgánica no mineralizada denominada cementoide. Posteriormente, el cementoide se mineraliza gradualmente por precipitación de cristales de hidroxiapatita, conformando las primeras capas de cemento acelular primario.
Reabsorción Radicular
La reabsorción radicular (incluso en enfermedades sistémicas que provocan reabsorción ósea) es infrecuente en la dentición permanente, a diferencia del hueso, que sufre un continuo proceso de remodelación. No se conoce el mecanismo exacto por el cual la raíz es resistente a la reabsorción.
Factores que Influyen en la Reabsorción
La hipótesis más aceptada se basa en que el cemento y la predentina son esenciales en la resistencia de la reabsorción radicular, ya que los osteoclastos no se adhieren a la matriz desmineralizada. Los osteoclastos se unen a proteínas extracelulares RGD (que contienen arginina-glicina-ácido aspártico). Estos péptidos RGD se unen a los cristales de calcio de las superficies mineralizadas, actuando como nexo de unión a los osteoclastos.
Como ya dijimos, la parte más externa del cemento está cubierta por una capa de cementoblastos, situada sobre la superficie cementoide desmineralizada, por lo que no presentan una superficie adecuada para que el osteoclasto se adhiera. De ahí que la ausencia de proteínas RDG en el cemento y predentina, reduzca la posibilidad de adhesión de los osteoclastos, confiriéndole a la raíz más resistencia a la reabsorción.
Algunos estudios apoyan esta teoría, además de corroborarse clínicamente, pues en las luxaciones en las que se pierde parte del cemento, la reabsorción radicular aparece pronto. Un gran número de mediadores, como hormonas, integrinas, factores de transcripción y citocinas, afectan a la función osteoclástica. Se sabe que los mediadores inflamatorios son potentes estimuladores de los osteoclatos y de los odontoclastos.
Por todo ello, la resistencia a sufrir reabsorción radicular (incluso con infección) radica en la integridad del precemento y la predentina. Si como consecuencia del trauma se alteran, la inflamación provoca una reabsorción radicular.
Enfermedades y Condiciones Asociadas al Cemento Radicular
Existen diversas condiciones patológicas que pueden afectar el cemento radicular:
- Hipercementosis: Caracterizada por deposición excesiva de cemento, principalmente en la región apical y menos frecuentemente en toda la superficie radicular. Radiográficamente se observa como ensanchamiento apical o radicular generalizado con mantenimiento del espacio periodontal. Aunque generalmente asintomática, puede complicar procedimientos endodónticos o exodoncias.
- Reabsorción radicular externa: Implica la pérdida progresiva de cemento y posteriormente dentina por actividad osteoclástica.
- Reabsorción por reemplazo (anquilótica): donde el cemento es progresivamente sustituido por hueso, eliminando el ligamento periodontal.
- Cementículos: Masas globulares de cemento, libres o adheridas a la superficie radicular, frecuentemente localizadas en el ligamento periodontal cerca del ápice.
- Cementoblastoma: Neoplasia odontogénica benigna rara, caracterizada por proliferación de tejido similar al cemento fusionado a la raíz dental. Radiográficamente aparece como masa radiopaca rodeada por halo radiolúcido, fusionada a la raíz y causando frecuentemente reabsorción radicular.
- Exposición cementaria: La recesión gingival expone cemento que normalmente está cubierto por encía. Este cemento expuesto es más susceptible a desgaste mecánico, caries radicular y sensibilidad dental.
Innovaciones en la Regeneración del Cemento
En regeneración periodontal, el descubrimiento de proteínas derivadas de la matriz del esmalte (Emdogain®) ha revolucionado las aproximaciones terapéuticas. Estas proteínas, principalmente amelogeninas, recapitulan procesos del desarrollo embriológico, estimulando la diferenciación de cementoblastos y la formación de nuevo cemento acelular con inserción funcional de fibras.
Las terapias celulares basadas en células madre mesenquimales del ligamento periodontal (PDLSC) o células progenitoras del folículo dental muestran potencial para diferenciarse en cementoblastos funcionales.
Factores de crecimiento específicos como proteínas morfogenéticas óseas (BMP-2, BMP-7), factor de crecimiento derivado de plaquetas (PDGF) y factor de crecimiento transformante-β (TGF-β) han demostrado capacidad para estimular la cementogénesis.
Técnicas de biomodificación radicular mediante agentes como tetraciclinas, ácido cítrico o EDTA buscan descontaminar la superficie radicular y exponer la matriz colágena del cemento, facilitando la adhesión celular y la inserción de nuevas fibras.