Las células madre están consideradas como uno de los futuros más prometedores de la Medicina. Actualmente se están desarrollando investigaciones para su estudio y para determinar sus posibles aplicaciones.
El objetivo de esta revisión es actualizar los conocimientos sobre las células madre dentarias, sus aplicaciones (actuales y futuras) y la controversia en cuanto a su utilización.
Células Madre: ¿El futuro de la regeneración dental?
I. Concepto y Clasificación de las Células Madre
Hay múltiples formas de clasificación de las C.M. (Células Madre). Las células madre tienen capacidad para autorenovarse, ser clonogénicas y diferenciarse en distintas estirpes celulares, teniendo la capacidad osteo/odontogénica, adipogénica y neurogénica.
Según el origen, se clasifican en:
- Origen embrionario: Poseen la capacidad de diferenciarse en cualquier tipo de célula (totipotentes), contando así con un enorme potencial para la regeneración tisular.
- Origen adulto: También son denominadas células madre postnatales. Son multipotentes y sobre ellas cabe destacar que su potencial de diferenciación queda restringido a la capa embrionaria de la que procedan. Las MSC (mesenchymal stem cells) fueron aisladas por primera vez en aspiraciones de médula ósea. Hoy en día sus marcadores continúan siendo la clave en cuanto al aislamiento de células madre.
Según el potencial de diferenciación:
- C.M. totipotentes: Son aquellas capaces de originar un embrión y un individuo completo, diferenciándose hacia cualquier estirpe celular.
- C.M. pluripotentes: Tienen la capacidad de poder desarrollar los 200 tejidos de un ser humano pero no el tejido extraembrionario.
- C.M. multipotentes: Pueden originar un subconjunto de tipos celulares.
- C.M. oligopotentes: Al igual que las anteriores, pueden desarrollar un conjunto de tipos de celulares, pero mucho más reducido.
- C.M. unipotentes.
II. Células Madre de Origen Dental: Concepto y Clasificación
Las Células Madre Dentales (C.M.D.) son C.M. que poseen potencial de multidiferenciación y por tanto pertenecen al grupo de C.M. adultas, teniendo la capacidad de formar células con carácter osteo/odontogénico, adipogénico y neurogénico. Sin embargo, se puede afirmar que, en comparación con las C.M.
Existen diversos tipos de células madre de origen dental:
1. Células Madre de la Pulpa (Dental Pulp Stem Cells (DPSC))
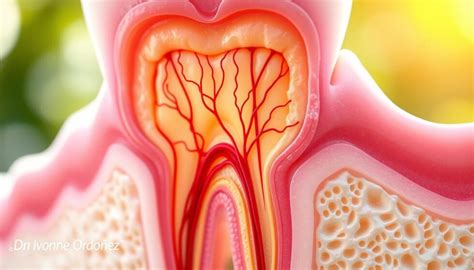
Fueron las primeras células madre dentarias que se aislaron (Gronthos 2000). Por analogía con las células madre de la médula, se consideró que había una comunidad de células multipotenciales en el tejido pulpar de dientes maduros (6). El origen y localización exacta de estas células sigue siendo incierto (Figura 1). La producción de DPSC es muy pequeña (1 por 100 de todas las células) y según aumenta la edad del individuo, la disponibilidad de estas células se ve reducida. Se han estudiado sobretodo las células que provienen de terceros molares y dientes supernumerarios. Cabe destacar que, si son aisladas durante la formación de la corona, las DPSC son más proliferativas que si se aíslan más adelante. De cara a un uso terapéutico ha de tenerse en cuenta su interacción con biomateriales.
La capacidad de diferenciación de las DPSC quedó demostrada en estudios experimentales en ratas, donde se pudo observar su potencial terapéutico para la reparación de un infarto de miocardio inducido tras ligadura de las arterias coronarias. Las SBP-DPSCs son otra subpoblación de DPSCs capaces de diferenciarse hacia osteoblastos, sintetizando chips de tejido óseo tridimensionales in vitro que se pueden diferenciar en osteoblastos y en endoteliocitos. Su asombrosa capacidad de diferenciación les permite dar lugar in vivo a hueso adulto con canales de Havers y la apropiada vascularización (9).
2. Células Madre del Ligamento Periodontal (Periodontal Ligament Stem Cells (PDLSC))
Varios estudios afirman que el ligamento periodontal tiene poblaciones de células que pueden diferenciarse tanto hacia cementoblastos como hacia osteoblastos (Tabla 1). La presencia de múltiples tipos de células en el periodonto sugiere que este tejido contiene C.M. llamadas PDLSC (Periodontal Ligament Stem Cells) que mantienen la homeostasis y la regeneración del tejido periodontal. Las fibras colágenas generadas in vivo en humanos, fueron capaces de unirse con la nueva estructura formada de cemento, imitando así la unión fisiológica de las fibras de Sharpey.
Una de las más prometedoras investigaciones con PDLSCs es la que las vincula a la hipoplasia congénita radicular, una enfermedad caracterizada por ser un desorden evolutivo fisiológico de la raíz que cursa con displasia ectodérmica, movilidad dentaria, atonía masticatoria y exfoliación prematura. Se sabe que el gen ADAM28 se expresa en el gérmen dentario, las células de la papila dental y las células del folículo dental, y se supuso que estaría involucrado en el proceso morfogénico tanto de la corona como de la raíz. Se estudió la influencia del gen ADAM28 en la proliferación, apoptosis y diferenciación de las PDLSCs en terceros molares impactados.
3. Células Madre de Dientes Temporales Exfoliados (Stem cells from Human Exfoliated Deciduous teeth (SHED))
Se han aislado células de la pulpa remanente de los dientes deciduos exfoliados, denominadas SHED. Conservadas (Figura 2), las SHED se consideran una importante fuente de células madre de fácil obtención. Los dientes deciduos y los permanentes tienen importantes diferencias en cuanto a su función, proceso de desarrollo y estructura tisular, y al comparar las SHED con las DPSC, se encontró una mayor velocidad de proliferación y una mayor capacidad de especialización. Un revelador ejemplo es el de la existencia, hasta ahora ignorada, de células epiteliales en la pulpa de estos dientes. También se ha probado el potencial de las SHED para diferenciarse en células angiogénicas, cuya capacidad de inducción se considera fundamental para cualquier tipo de regeneración con tejido conjuntivo. En cuanto a la capacidad osteoinductora, se ha comprobado, en ratones, que las SHED pueden reparar defectos de formación ósea (Tabla 1).
4. Células Madre de la Papila Apical (Stem Cells from Apical Papilla (SCAP))
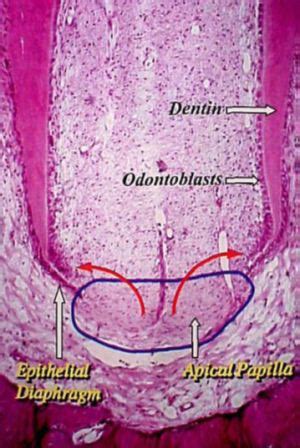
La papila apical hace referencia al tejido blando situado en los ápices del diente permanente que se está formando. Existe una zona muy rica en células entre la papila apical y la pulpa. Parece que las SCAP son las precursoras de los odontoblastos primarios, responsables de la formación de la dentina radicular, mientras que las células madre de la pulpa (DPSC) son, probablemente, las precursoras de los odontoblastos que forman la dentina reparativa (5). Además, éstas últimas, contienen un mayor componente vascular y celular que las SCAP.
5. Células Madre del Folículo Dental (Dental Follicle Precursor Cells (DFPC))
El folículo dental es un tejido ectomesenquimal que rodea el órgano del esmalte y la papila dental del germen del diente permanente en formación. Este tejido contiene C.M., que son las que acabarán formando el periodonto, constituido por cemento, ligamento, hueso alveolar y encía. Las DFPC han sido aisladas de los folículos dentales de los terceros molares impactados. In vitro, estas células muestran una morfología típica de fibroblastos. Después de inducción, se ha demostrado diferenciación osteogénica. In vivo se ha identificado el antígeno STRO-1 en los folículos dentales. El trasplante de estas células genera una estructura constituida de tejido fibroso rígido. No se ha observado ni dentina, ni cemento, ni formación ósea en el trasplante in vivo (Tabla 1).
III. Aplicaciones Clínicas en Odontología
La ingeniería tisular basada en C.M.D tiene un futuro prometedor dentro de las ciencias sanitarias. Se han descrito evidencias en las que células madre de tejido no neural pueden ser capaces de diferenciarse en células neurales. Las células madre de la pulpa son capaces de producir factores neurotróficos e incluso rescatar motoneuronas después de una lesión de la médula espinal. Por tanto, podrían ser un recurso importante para reparar lesiones de tejidos dentarios, inducir regeneración ósea y posiblemente tratar lesiones del tejido nervioso o incluso enfermedades degenerativas.
1. Cirugía (regeneración e implantología)
Los implantes se han convertido en una de las terapéuticas más frecuentes en la presente década. El mayor problema de la técnica implantológica, reside en su falta de contorno natural y la relación con el hueso alveolar: no tiene ligamento periodontal. Estudios in vivo en perros, tras la obtención de células del germen dentario en estadio de campana, demuestran que, aisladas e implantadas en otro alveolo, regeneran la estructura dentinaria, pero no el esmalte ni la raíz. En cerdos, implantadas de nuevo en su alveolo original, se observó que había formación de la raíz y el periodonto. En lugar de regenerar un diente completo, las células de la papila apical (SCAP) y las del ligamento (PDLSC) se han utilizado para generar una raíz biológica, junto con el tejido periodontal adyacente. Tras 3 meses, en un cerdo, se observó que se había formado la raíz en la mandíbula y posteriormente se le sometió a la inserción de una corona de porcelana. El tejido periodontal había rodeado a la raíz, y aparentemente tenía una relación natural y biológica con el hueso que lo rodeaba. Sin embargo, la fuerza mecánica que poseía esta raíz, era un tercio menor que aquellas raíces naturales, debido a la presencia de hidroxiapatita residual, ya que no se generó el mismo tipo de dentina que la formada en un diente natural. A partir de DPSC procedentes de los terceros molares superiores extraídos previamente y de un andamiaje a base de colágeno, se creó un biocomplejo que restauró los defectos mandibulares. La óptima regeneración ósea fue evidente tras un año del injerto (17).
2. Endodoncia (apicogénesis y apicoformación)
La ingeniería del tejido pulpar (Mooney et al., 1996) es un campo que está en continua expansión y que tiene como objetivo el reemplazo de una pulpa inflamada, necrótica e irreversible por una pulpa sana y un tejido funcionalmente competente, capaz de formar nueva dentina. Tal tratamiento es atractivo para dientes inmaduros necróticos, en los que es necesario completar el desarrollo radicular. La capacidad de las C.M.D. El cierre del ápice dentario tiene lugar unos 3 años de media después de la erupción del diente (apicogénesis). La repoblación del ápice abierto, propio de los dientes inmaduros, con células madre capaces de ser dirigidas hacia una estirpe tisular concreta y que regeneren el tejido natural podría suponer una nueva alternativa de tratamiento para los pacientes que han sufrido un gran daño en algún diente inmaduro. Una combinación de las C.M. La revascularización se ha estudiado in vitro y la aplicación de factores de crecimiento angiogénicos, aumentaron las condiciones favorables del entorno para una curación adecuada. Estudios periodontales muestran que las células pueden proliferar y migrar desde el ligamento sano adyacente, hasta el área dañada. Esto sugiere que las PDLSC puedan ser estimuladas a distancia, para que migren hasta el ápice inmaduro de la raíz. Es interesante recalcar que se han encontrado un mayor número de C.M.
Los problemas que nos encontramos son los siguientes:
- ¿Qué señales del entorno son necesarias para que se dé este proceso? y ¿cuál es el nivel crítico inflamatorio necesario para estimular la migración de las células madre hacia el ápice abierto, con el potencial de depositar dentina, cemento y/o hueso alveolar pero sin dañar irreversiblemente las células?
- La regeneración in vitro: las células tienen que crecer y expandirse antes de ser implantadas en el canal radicular. Las células implantadas deben adherirse a las paredes desinfectadas del canal, lo cual puede significar un cambio en el actual abordaje de la endodoncia.
Por último, el tejido implantado carece de soporte vascular, y además es una técnica muy difícil de realizar sin daño celular.
Además del mismo modo que se intentaba regenerar el ligamento periodontal en el caso de las aplicaciones quirúrgicas, los intentos para regenerar la pulpa están siendo estudiados. Antes se proponía la inducción de una hemorragia y que se creasen coágulos para que sirviesen de guía en la reparación tisular, pero se formaba escasamente 1mm de tejido, que ni siquiera era pulpar. Aún no se ha conseguido la regeneración pulpar completa.
IV. Investigación Actual y Obtención de C.M.D.
Actualmente en España nos regimos bajo la legislación aprobada por la Unión Europea. En 2001, el Programa Marco de Investigación aporta 50.000 millones de euros para investigaciones en el periodo comprendido entre 2007-2013. En EE.UU. Se han realizado diversos estudios destinados a conseguir el aislamiento, caracterización y diferenciación celular de C.M.D. procedentes de dientes deciduos exfoliados, supernumerarios, terceros molares o dientes extraídos por razones ortodóncicas que demuestran que las DPSC:
- Se pueden aislar mediante métodos de cultivo celular para obtener colonias clonogénicas, obteniendo una morfología característica de las C.M. post-natales (semejantes a fibroblastos, alargadas y aplanadas, ubicadas en estas colonias).
- Poseen marcadores de membrana específicos de células progenitoras mesenquimales: STRO-1 y CD-44.
V. Consideraciones Éticas
Es importante conocer tanto los beneficios como los riesgos que aporta la investigación sobre C.M. Su empleo puede convertirse en una práctica diaria en un futuro próximo.
En cuanto a cuestiones éticas, los principales problemas que encuentra la investigación de células madre son:
- Ante estas situaciones, existen implicaciones de carácter ético, moral y religioso que se oponen a la investigación con células madre, si bien los sectores más radicales parecen escandalizarse en menor medida con aquellas de tipo adulto.
Tabla 1 - Nombres, abreviaturas y características in vitro e in vivo más importantes de las células madre de origen dentario. Debemos tener en cuenta que las características in vitro varían en mayor o menor medida, dependiendo del tipo de célula.
| Célula Madre | Abreviatura | Características In Vitro | Características In Vivo |
|---|---|---|---|
| Células Madre de la Pulpa Dental | DPSC | Alta proliferación, diferenciación osteogénica | Reparación de infarto de miocardio (en ratas) |
| Células Madre del Ligamento Periodontal | PDLSC | Diferenciación hacia cementoblastos y osteoblastos | Regeneración del tejido periodontal |
| Células Madre de Dientes Temporales Exfoliados | SHED | Mayor velocidad de proliferación, diferenciación angiogénica | Reparación de defectos de formación ósea (en ratones) |
| Células Madre del Folículo Dental | DFPC | Morfología de fibroblastos, diferenciación osteogénica | Formación de tejido fibroso rígido |