El sarro dental, también llamado cálculo dental o tártaro, es un depósito duro de color amarillento o marrón que se forma sobre la superficie de los dientes por la mineralización de la placa bacteriana (biofilm oral). En la práctica odontológica moderna, el sarro reviste gran importancia debido a su alta prevalencia (afecta hasta ~90% de la población) y a su relación directa con enfermedades gingivales y periodontales.
Su presencia proporciona una superficie rugosa y porosa donde se adhieren nuevas bacterias patógenas, contribuyendo a la gingivitis y, si no se controla, a la periodontitis (destrucción de los tejidos de soporte dental).
007 CÓMO SE PUEDE PREVENIR LA FORMACIÓN DE SARRO EN LOS DIENTES
Composición Química del Sarro Dental
El sarro dental se compone aproximadamente de un 70-80% de material inorgánico (principalmente cristales de fosfato de calcio) y un 20-30% de material orgánico. Entre los componentes inorgánicos predominan minerales como la hidroxiapatita, la whitlockita, el fosfato octacálcico y la brushita, que le confieren su dureza característica.
Estos cristales se forman al precipitar los iones de calcio (Ca2+) y fosfato (PO43-) presentes en la saliva o en el fluido crevicular de las encías. La porción orgánica del cálculo incluye bacterias muertas encapsuladas en una matriz de polisacáridos, proteínas salivares absorbidas selectivamente y restos orgánicos del biofilm original.
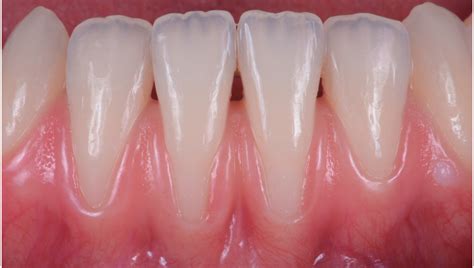
Ejemplo de sarro dental en incisivos inferiores
Tipos de Sarro Dental
El sarro dental se clasifica principalmente en dos tipos según su ubicación:
- Sarro supragingival: Depósito visible por encima del margen de la encía, sobre la corona del diente. Suele presentar un color blanquecino o amarillento y una consistencia calcárea. Se forma con mayor frecuencia en las superficies dentales expuestas a la saliva de las glándulas salivales mayores (por ejemplo, cara lingual de los incisivos inferiores y cara bucal de molares superiores), donde la saliva aporta minerales que precipitan sobre la placa bacteriana.
- Sarro subgingival (infragingival): Depósito que se encuentra por debajo de la línea de la encía, adherido a las raíces dentales dentro del surco o bolsa periodontal. Suele ser de color marrón oscuro o negruzco debido a la incorporación de pigmentos sanguíneos y productos de la inflamación gingival. Sus minerales provienen en parte del fluido crevicular gingival y la sangre (en lugar de la saliva), lo que contribuye a una composición ligeramente distinta. El sarro subgingival suele ser más denso y está íntimamente asociado a la enfermedad periodontal avanzada, ya que se acumula en zonas de inflamación crónica de las encías.
Textura y Adherencia del Sarro
Independientemente de su ubicación, la superficie del sarro es áspera y porosa, ofreciendo nichos donde las bacterias pueden alojarse y protegerse. Esta rugosidad facilita la colonización bacteriana continua, creando un ciclo en el que sobre el sarro existente se forma nueva placa que a su vez puede mineralizarse.
El cálculo se adhiere firmemente al esmalte dental o a la superficie radicular (cemento) mediante fuerzas físicas (fuerzas de Van der Waals, adhesión mecánica a las irregularidades del diente) y químicas. Con el tiempo, penetra en las irregularidades microscópicas del diente, lo que dificulta aún más su eliminación.
Formación del Sarro Dental
El sarro dental se origina a partir de la placa bacteriana, que es un biofilm blando compuesto por bacterias vivas, polisacáridos y restos orgánicos adherido a la superficie dental. Inicialmente, tras una limpieza dental, las proteínas de la saliva forman una película adquirida sobre el diente en pocas horas.
Sobre esta película, las bacterias comienzan a colonizar y formar microcolonias en 24-48 horas, produciendo una matriz extracelular que las rodea. Si la placa bacteriana no se remueve de manera rutinaria, en cuestión de días empieza a sufrir calcificación por la deposición de minerales disueltos en la saliva.
Las bacterias del biofilm modifican el microambiente: consumen nutrientes y producen subproductos que pueden alterar el pH local. En condiciones favorables (pH neutro o ligeramente alcalino), los cristales de fosfato cálcico comienzan a precipitar en la matriz de la placa, endureciéndola gradualmente.
La presencia de ciertas bacterias y sus productos es crítica en la formación de sarro. Las bacterias del biofilm dental concentran iones minerales del medio: por ejemplo, metabolizan proteínas y urea liberando amoníaco, lo que eleva el pH local y favorece la precipitación de calcio y fosfato.
Además, durante la inflamación gingival las bacterias estimulan la liberación de enzimas como la fosfatasa alcalina (de células del huésped), que descomponen compuestos fosforados orgánicos liberando más fosfato inorgánico en el entorno. La combinación de un aumento en la concentración de calcio/fosfato y un pH más alcalino crea las condiciones ideales para la cristalización sobre la placa dental.
A medida que el biofilm se mineraliza, muchas bacterias quedan atrapadas y mueren, quedando sus células incrustadas en la masa de sarro. Sin embargo, la capa externa del cálculo suele estar cubierta por placa no mineralizada activa, manteniendo un frente bacteriano en contacto con el tejido gingival.
Algunos microorganismos, como Actinomyces spp. y Veillonella, se han asociado a la formación de cálculo por su capacidad de crear un ambiente alcalino, mientras que otros (p.ej. Streptococcus mutans) contribuyen más a la formación de placa acidogénica (asociada a caries) que a la calcificación.
Factores Influyentes en la Formación del Sarro
No solo las bacterias per se influyen en la formación del sarro; también intervienen factores del huésped como la composición de la saliva y la respuesta inmune local. La saliva de cada individuo posee concentraciones variables de minerales (calcio, fosfatos, fluoruro), proteínas (por ejemplo, estaterina, prolina) y capacidad tampón que afectan la velocidad de calcificación.
Por ejemplo, una saliva con alto contenido de calcio y pH elevado puede promover una calcificación más rápida de la placa. Estudios recientes han encontrado diferencias en el proteoma salival entre formadores rápidos de sarro y formadores lentos, sugiriendo que ciertas proteínas salivares y propiedades físico-químicas de la saliva modulan la tendencia a acumular cálculo.
El sistema inmunitario local en las encías también desempeña un papel. Durante la inflamación gingival, los neutrófilos liberan trampas extracelulares de neutrófilo (NETs), estructuras de ADN y enzimas diseñadas para atrapar bacterias. Investigaciones recientes indican que estas NETs pueden convertirse en un andamiaje que facilita la calcificación dentro del biofilm, contribuyendo a la formación de sarro.
Es decir, componentes de la respuesta inmune (como el ADN de neutrófilos muertos) se integran a la placa y actúan como núcleos de cristalización.
Detección y Diagnóstico del Sarro Dental
La detección del sarro dental es parte rutinaria del examen odontológico. El sarro supragingival suele diagnosticarse por inspección visual - se observa como depósitos duros amarillentos o marrones adheridos a los dientes, que pueden teñirse con reveladores de placa.
El sarro subgingival, al estar oculto bajo la encía, se detecta palpando con un explorador periodontal (que “raspa” la raíz indicando su presencia) o mediante radiografías interproximales, en las que el cálculo aparece como zonas opacas adjuntas a la superficie radicular.
Los dentistas y higienistas dentales registran la localización y cantidad de sarro durante la evaluación periodontal, ya que su presencia se asocia con profundidades de sondaje mayores y sangrado gingival.
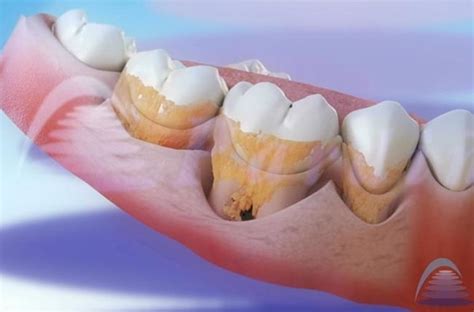
Detección de sarro subgingival
Tratamiento del Sarro Dental
Debido a que el sarro adherido no puede ser eliminado con métodos de higiene oral casera, su tratamiento principal es la remoción profesional a través de la limpieza dental.
Profilaxis Dental
La profilaxis dental es el procedimiento preventivo en el cual el odontólogo o higienista elimina el sarro supragingival y la placa acumulada, generalmente en pacientes con encías sanas o gingivitis leve. Esta limpieza profesional incluye típicamente raspado dental y pulido: primero se usa instrumental manual (curetas, instrumentos de escariado) y/o dispositivos ultrasónicos para desprender los depósitos de cálculo, y luego se pulen las superficies dentales con pastas abrasivas para retrasar la recolonización.
En casos de depósitos supragingivales leves, la profilaxis puede realizarse sin anestesia y en una sola sesión, enfocándose en las zonas habituales de acumulación (dientes anteriores inferiores, molares superiores, bordes gingivales). Es un procedimiento seguro y rutinario, esencial para prevenir la progresión de la gingivitis a enfermedad periodontal.
Raspado y Alisado Radicular (RAR) o Curetaje Periodontal
Cuando existe sarro subgingival significativo asociado a periodontitis, es necesario un tratamiento más profundo llamado raspado y alisado radicular (RAR) o curetaje periodontal. Este procedimiento consiste en eliminar todo el cálculo adherido a las raíces dentales por debajo de la encía, junto con la placa bacteriana subgingival y el cemento dental contaminado, seguido de un alisado de la superficie radicular para retardar nueva colonización.
Dado que el sarro subgingival suele estar fuertemente adherido e incluso penetrado en las irregularidades radiculares, el RAR suele realizarse bajo anestesia local por cuadrantes (secciones de la boca) para mayor comodidad del paciente. Se emplean curetas periodontales especializadas y dispositivos ultrasónicos de insertos delgados que permiten alcanzar el fondo de las bolsas periodontales.
El objetivo es dejar la raíz limpia y lisa, lo que favorece la readherencia de la encía y la cicatrización. El raspado y alisado radicular es un pilar del tratamiento periodontal en pacientes con periodontitis incipiente a moderada, y numerosos estudios demuestran su efectividad en reducir la inflamación y detener la progresión de la pérdida ósea periodontal cuando se elimina exhaustivamente el sarro subgingival.
Cirugía Periodontal de Acceso
En situaciones de periodontitis avanzada, donde existen bolsas periodontales profundas (>5 mm) y acumulación de sarro persistente, puede requerirse una cirugía periodontal de acceso para eliminar completamente el cálculo. Procedimientos como la cirugía de colgajo (levantamiento quirúrgico de la encía) permiten visualizar y acceder directamente al sarro subgingival remanente en las raíces para removerlo bajo visión directa, seguido de un alisado radicular minucioso.
Esta intervención se reserva para casos en que el raspado cerrado (no quirúrgico) resulta insuficiente para eliminar el cálculo debido a la profundidad o localización complicada. Tras la cirugía de acceso y desbridamiento, la encía se reposiciona ajustada al diente, reduciendo la profundidad de bolsa y facilitando el control futuro de placa.
Otras técnicas quirúrgicas asociadas pueden incluir la gingivectomía (recorte de encía) en casos de agrandamiento gingival con abundante sarro subgingival, o la regeneración tisular guiada si hay defectos óseos significativos (además de la eliminación del cálculo). En todos los casos, la eliminación completa de los depósitos de sarro es un objetivo fundamental para restablecer la salud periodontal.
Tecnologías Avanzadas para la Eliminación del Sarro
Si bien los escaladores ultrasónicos convencionales son efectivos para fracturar y desprender el sarro, pueden llegar a producir microrayaduras o desgaste en la superficie del diente. Para abordar este inconveniente, se han desarrollado sistemas alternativos como los chorros de agua pulsátil de alta precisión.
Un ejemplo es el actuador de chorro de agua pulsado (ADPJ), un dispositivo que genera un chorro a presión controlada capaz de eliminar selectivamente el cálculo según su dureza, sin dañar el esmalte adyacente. Estas tecnologías de hidrodinámica inducida han mostrado reducir significativamente la cantidad de sarro sin evidenciar daño en la superficie dental, ajustando la presión del chorro según la necesidad.
Asimismo, se investigan puntas ultrasónicas de nueva generación con recubrimientos especiales (p.ej. diamante o nitruro de titanio) y frecuencias moduladas que optimizan la remoción de sarro minimizando el daño al diente.
Terapias Láser en Periodoncia
El uso de láseres dentales se ha explorado como alternativa o complemento para eliminar el sarro y desinfectar las bolsas periodontales. En particular, los láser de erbio (Er:YAG y Er,Cr:YSGG) pueden pulverizar los depósitos de cálculo por ablación, logrando superficies radiculares prácticamente libres de sarro detectable.
Esta técnica láser genera microexplosiones y ondas de choque que pueden desorganizar el biofilm calcificado y matar bacterias residuales. No obstante, los estudios han encontrado ciertas limitaciones: la ablación láser exclusiva puede dejar la superficie radicular más rugosa que el raspado mecánico tradicional, y existe riesgo de daño térmico a los tejidos (aumento de temperatura en la dentina y la pulpa).
Por ello, la terapia combinada es la más recomendada: el láser se utiliza tras el raspado convencional para eliminar restos microscópicos de sarro y desinfectar, mientras que el grosor principal del cálculo se retira con métodos mecánicos. De esta forma, se aprovechan las ventajas del láser (mayor desinfección y acceso a recovecos) sin comprometer la integridad de la raíz.
Tecnologías láser adyuvantes, como la fotoacústica o la fluorescencia láser, también se emplean experimentalmente para detectar sarro subgingival (el cálculo puede emitir fluorescencia bajo ciertas longitudes de onda, ayudando a guiar su eliminación).
Agentes Químicos y Pastas Dentífricas Antisarro
Paralelamente a la remoción mecánica, existe interés en prevenir o reducir la formación de sarro mediante compuestos que interfieran en la mineralización de la placa. Los dentífricos antisarro comerciales suelen incluir pirofosfatos, zinc u otros inhibidores de cristalización que se unen al calcio en la saliva, dificultando su depósito en los dientes.
Estos agentes han demostrado disminuir la acumulación de nuevo cálculo supragingival en pacientes con tendencia al sarro, aunque no eliminan el ya formado. Investigaciones recientes exploran sustancias novedosas: por ejemplo, el uso de aragonita (un mineral derivado del carbonato de calcio presente en conchas marinas) en pastas dentales experimentales ha mostrado eficacia en remover depósitos superficiales de sarro y prevenir su re-formación, sin provocar desgaste del esmalte.
Asimismo, se están probando compuestos derivados de plantas con propiedades antimicrobianas y anti-biofilm para inhibir la maduración de la placa antes de que calcifique (por ejemplo, extractos de té verde, enzimas como la dextranasa y mutanasa, etc.).
Nanotecnología y Terapias Dirigidas al Biofilm
Una de las fronteras de la odontología preventiva es el uso de nanopartículas y biotecnología para controlar el biofilm oral antes de que forme sarro. Nanopartículas de metales como plata y oro poseen propiedades antibacterianas; su incorporación en cepillos dentales o recubrimientos podría ayudar a reducir la formación de placa y cálculo.
Además, se investigan enzimas y péptidos antimicrobianos diseñados para desorganizar selectivamente la matriz del biofilm o inhibir la adhesión bacteriana a los dientes. Estas terapias dirigidas al biofilm podrían complementar las estrategias convencionales de higiene oral y reducir la necesidad de intervenciones más invasivas contra el sarro.
Cristales de Whitlockita
En la zona transparente o translúcida, la dentina intertubular está también desmineralizada parcialmente. Hay una característica importante y es que los túbulos dentinarios están llenos de cristales de whitloquita. Estos cristales son de gran tamaño y más resistentes al ataque ácido. Esta esclerosis tubular es la responsable de su aspecto transparente o translúcido.
Los depósitos intratubulares no se sabe con certeza si son un mecanismo de defensa activo o el resultado de un fenómeno cíclico de disolución y precipitación de los cristales. Lo que sí se ha demostrado es que su presencia disminuye la permeabilidad dentinaria y, por tanto, el paso de ácidos, bacterias y productos bacterianos, sirviendo de protección para el tejido pulpar. Por estos motivos es una dentina que debemos respetar durante la remoción de la caries.
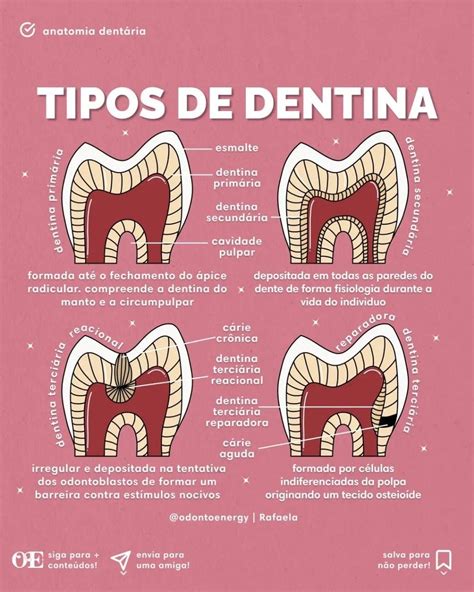
Tipos de dentina
Algunos autores denominan a la dentina transparente dentina esclerótica, de hecho, clínicamente se describía como una dentina más dura a la exploración. Sin embargo, aunque el interior de los túbulos está ocupado por cristales de whitloquita, como ocurre en la dentina esclerótica, es una dentina significativamente más blanda. Esto se debe a que su matriz intertubular está desmineralizada como consecuencia del proceso carioso y, como ya ha sido demostrado, las propiedades mecánicas de la dentina dependen de las de la dentina intertubular.
Adhesión a la dentina afectada por caries
Si revisamos la literatura, los datos referentes a la resistencia adhesiva en dentina afectada por caries son escasos. Esta ausencia de información se debe a que los diferentes tests disponibles necesitaban evaluar áreas extensas y uniformes, circunstancia que es imposible de conseguir en dentina afectada por caries.
El desarrollo de la técnica de microtensión permitió evaluar áreas adhesivas cercanas al milímetro cuadrado y, basándose en esta metodología, Nakajima pudo medir de forma selectiva la resistencia a la tensión en la dentina afectada por caries, áreas que se caracterizan por ser irregulares y pequeñas.
En sus diferentes estudios compararon la eficacia adhesiva obtenida con diferentes sistemas adhesivos en molares cariados, distinguiendo los valores obtenidos en la dentina afectada por caries y en la dentina sana procedente de un mismo espécimen. Para distinguir la dentina infectada de la afectada utilizaban fucsina básica y tras realizar el test de microtensión, determinaban la microdureza de cada espécimen para certificar si era o no dentina afectada. En sus estudios también observaron las características morfológicas de la interfase generada para cada tipo de adhesivo y dentina con microscopía electrónica de barrido.
Los hallazgos más significativos de dichos estudios pueden resumirse de la siguiente forma:
- Los valores de resistencia adhesiva son inferiores en dentina afectada por caries, comparados con los obtenidos en dentina sana procedentes ambas de los mismos especimenes.
- El grosor de la capa híbrida formada en dentina afectada por caries es mayor. Esto se debe a que la dentina está previamente desmineralizada, por lo que los adhesivos pueden infiltrar una zona más profunda. Sin embargo, no se corresponden el grosor de esta capa con la resistencia adhesiva obtenida.
- La microdureza de la dentina afectada por caries es siempre significativamente inferior a la de la dentina sana, a pesar de que los túbulos dentinarios estén obliterados por cristales minerales.
- Los autores recomiendan realizar una técnica de grabado total con ácido ortofosfórico en concentraciones entre el 32-37%, puesto que consiguen remover de forma más efectiva los cristales intratubulares y, por tanto, mayor formación de tags de resina principales y laterales, que cuando utilizan concentraciones menores (10%).
- Los resultados obtenidos ponen de manifiesto que la técnica de adhesión húmeda mejora la adhesión establecida no sólo en dentina sana, sino también en dentina afectada por caries.
- Las nuevas formulaciones de los sistemas adhesivos, como son los que se presentan en una solo frasco, aportan mejores valores de resistencia adhesiva tanto en dentina sana como en la afectada por caries.
- La información sobre la resistencia adhesiva obtenida con los sistemas autograbadores es aún insuficiente. Los autores describen que el grosor de la capa híbrida también está aumentado, por lo que esta dentina es también permeable a los monómeros ácidos, puesto que está previamente desmineralizada por el proceso carioso y es más porosa.
Las posibles causas que justifican los valores inferiores obtenidos en la dentina afectada por caries son:
- El colágeno de la dentina afectada puede estar alterado por el proceso carioso o por efecto del grabado ácido.
- La dentina afectada está desmineralizada per se, por lo que el frente de desmineralización tras el grabado es mayor y los adhesivos quizá no lo infiltren completamente. Este hecho supondría que quedara una zona de dentina desmineralizada sin infiltrar y, por tanto, sensible a la degradación hidrolítica.
- Por último, los depósitos intratubulares dificultan la penetración de los monómeros y, por tanto, la formación de tags de resina con hibridación de las paredes intratubulares y de las ramificaciones laterales.
De acuerdo con la mayoría de los autores, para conseguir una adhesión estable y duradera al tejido dentinario se ha de formar una capa híbrida no sólo en la dentina intertubular, sino también en las paredes de los túbulos, circunstancias todas ellas que estarían dificultadas o imposibilitadas en esta dentina afectada.
Adhesión a dentina esclerótica
Estudios clínicos han puesto de manifiesto que las restauraciones de resina compuesta adheridas a dentina esclerótica o anciana muestran un porcentaje mayor de fracaso clínico. Esta dentina, que ha estado sometida a fenómenos de erosión, abrasión, atricción, abfracción o simplemente, como consecuencia del paso de los años, presenta una serie de características histopatológicas que condicionan este fracaso.
Al igual que la dentina afectada por caries, en la dentina esclerótica los túbulos dentinarios están obliterados por cristales de whitloquita, resistentes al ataque ácido, lo que condiciona que su permeabilidad esté reducida. Sin embargo, la dentina intertubular no está desmineralizada, sino todo lo contrario y, por encima de esta área hipermineralizada, se aprecia una capa de bacterias.
Los estudios que evalúan la resistencia adhesiva a esta forma de dentina alterada son escasos por los mismos motivos que fueron expuestos para la dentina afectada por caries. Y, al igual que ocurría con esta dentina, la modificación de la técnica de microtensión, en este caso por el Dr. Yoshiyama, permitió cuantificar la resistencia adhesiva en zonas de esclerosis.
Estos autores encontraron que los valores de resistencia adhesiva en dentina procedente de lesiones en cuña eran inferiores a los que obtenían en lesiones producidas artificialmente y achacaban este hecho a las características histológicas anteriormente descritas. La calcificación intratubular condicionaría la penetración intratubular de la resina adhesiva y la presencia de la capa hipermineralizada dificultaría la desmineralización y penetración posterior de la resina.
En cuanto a la morfología de la interfase generada en la dentina esclerótica, son muy interesantes los artículos de Prati y cols. y de Kwong y cols. Los autores describen que se produce una menor infiltración intratubular (tags de resina) por la presencia de cristales de whitloquita. Además, los tags de resina son anchos en sus primeras 3-4 micras, luego se estrechan mucho y, generalmente, son más cortos, correspondiéndose con un efecto más superficial del grabado ácido debido a la hipermineralización. Por los mismos motivos, rara vez se observan tags laterales. La hipermineralización superficial de la dentina intertubular ocasiona que las capas híbridas que se forman sean más delgadas.
tags: #cristales #de #whitlockita #dentina