La interpretación de las imágenes puntiformes hiperintensas múltiples en las secuencias ponderadas en T2 en la sustancia blanca cerebral ocupa una parcela muy importante en la práctica habitual del neurorradiólogo. Estas imágenes, detectadas a diario en los estudios de resonancia magnética (RM) cerebral del adulto, pueden ser indicativas de diversas condiciones, desde variantes normales hasta patologías graves.
Haciendo un paralelismo con el término unidentified bright objects (UBO), común en la bibliografía inglesa, presentamos el término «imágenes puntiformes hiperintensas en la sustancia blanca» (IPHSB), como una entidad semiológica que incluye cualquier caso en que contabilicen al menos 5 focos hiperintensos únicos de hasta un centímetro de diámetro máximo en las imágenes de RM obtenidas con secuencias ponderadas en T2, con o sin lesiones confluentes con un diámetro superior a un centímetro conjuntamente.
El principal objetivo de este artículo es tratar de facilitar el trabajo del radiólogo ante los casos de IPHSB para que pueda encuadrar los hallazgos dentro de un patrón predominante, de manera que la orientación diagnóstica sea más aproximada.
CLASE 10 TRASTORNOS DE LA SUSTANCIA BLANCA
Anatomía básica de la microcirculación cerebral
La microcirculación cerebral conforma una red vascular de anatomía muy compleja y variable según los individuos. Para tratar de entender los patrones de IPHSB propuestos es útil una aproximación básica a la anatomía microvascular cerebral.
Sistema microvascular arterial
Las arterias corticales atraviesan la corteza cerebral y profundizan en la sustancia blanca perpendicularmente a la superficie cortical, formando arteriolas terminales piales o medulares de hasta 4-5cm.
En su camino dan ramas cortas corticales que irrigan todo el espesor de la corteza cerebral y las fibras de sustancia blanca yuxtacortical (3-4mm), también denominadas fibras en «U», y establecen múltiples anastomosis que proporcionan a la corteza cerebral una rica red arteriolar.
Las arterias piales, en su trayecto profundo en la sustancia blanca, establecen muy pocas anastomosis capilares con las arteriolas piales vecinas, constituyendo unidades metabólicas arteriolares relativamente independientes.

Por otro lado, las arterias profundas subependimarias, que tienen su origen en las arterias coroideas, dan ramas penetrantes hacia la sustancia blanca, aunque su trayecto es más corto que el de las arterias piales.
Existe un segundo sistema terminal de arterias corticales y subependimarias (arterias lentículo-estriadas y tálamo-perforantes) que irrigan a los ganglios basales (GB).
Entre los sistemas arteriolares superficiales y profundos (arterias penetrantes piales y subependimarias) existen muy pocas anastomosis. Así pues, el parénquima situado en las áreas limítrofes entre la circulación superficial y profunda está menos vascularizado, mientras que las fibras en «U» presentan una mayor y mejor vascularización que el resto de la sustancia blanca y que los GB.
Sistema microvascular venoso
Las vénulas cerebrales, también llamadas vénulas medulares, se dividen en dos grandes grupos: vénulas medulares superficiales, que son canales venosos cortos que desde aproximadamente 1 o 2 cm por debajo de la corteza cerebral drenan hacia la superficie cortical; y las vénulas medulares profundas, que son canales más largos que drenan perpendicularmente a la superficie ventricular, hacia las venas subependimarias.
Existe un tercer grupo de vénulas transcerebrales, más escasas, que comunican ambos sistemas.
Espacio perivascular
Los sistemas arterial y venoso son anatómicamente bastante paralelos. El espacio perivascular rodea la pared de arterias y arteriolas (espacio de Virchow-Robin), y la de venas y vénulas (espacio perivenular), desde el espacio subaracnoideo hasta su trayecto intraparenquimatoso.
Las arteriolas superficiales o corticales están rodeadas por una hoja leptomeníngea que delimita la superficie vascular del espacio periarteriolar; la superficie parenquimatosa de este espacio está delimitado por la piamadre.
El endotelio de las arteriolas penetrantes de los GB está rodeado por dos capas leptomeníngeas que delimitan su espacio perivascular. El espacio perivenular, tanto superficial como profundo, aparentemente comunica directamente con el espacio subpial, sin hojas leptomeníngeas interpuestas.
Imágenes puntiformes hiperintensas «normales» en la sustancia blanca
La presencia en la RM de una pequeña cantidad de focos puntiformes hiperintensos en la sustancia blanca cerebral es un hallazgo muy habitual y, en una gran parte de casos, se puede considerar intrascendente. Estos puntos brillantes considerados «normales» pueden corresponder tanto a una dilatación de los espacios perivasculares como a pequeños focos glióticos o isquémicos lacunares.
En la RM convencional, los espacios perivasculares se observan dilatados (EPVd) en un 13% de los adultos sanos, y solo en el 3% de niños entre 20 meses y 16 años de edad. Los EPVd aparecen como focos lineales o fusiformes con la misma señal que la del líquido cefalorraquídeo en todas las secuencias.
Mientras que los espacios perivasculares pequeños (<2mm) se han considerado una variante anatómica, los espacios perivasculares de mayor tamaño (>2mm) se ha relacionado con el envejecimiento, la demencia, los estadios inflamatorios precoces en la esclerosis múltiple y la reacción inflamatoria en el traumatismo craneoencefálico.
Varios trabajos recientes han llegado a la conclusión de que los EPVd se asocian con lesiones isquémicas lacunares y, por tanto, este hallazgo puede considerarse un marcador de la enfermedad cerebrovascular de pequeño vaso.
La aparición de focos lacunares de aspecto isquémico en la sustancia blanca periventricular y subcortical es, asimismo, un proceso «fisiológico», puesto que se considera que la edad constituye, en sí misma, un factor de riesgo cerebrovascular. La presencia de lesiones en la sustancia blanca es prácticamente ubicua (95%) en mayores de 65 años.
Escala de Fazekas
Existen varias escalas visuales que permiten valorar las lesiones de la sustancia blanca relacionadas con el envejecimiento, o leucoaraiosis, con una buena correlación entre ellas. Una de las más conocidas es la de Fazekas, la cual ha sido incorporada a la escala ARWMC (age-related white matter changes), recomendada en caso de que no se pretenda cuantificar las lesiones de la sustancia blanca mediante TC o RM.
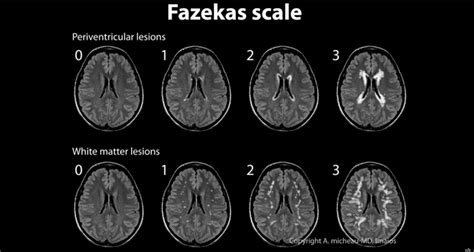
Esta escala contempla 4 grados de lesión microvascular puntiforme en la sustancia blanca: su ausencia corresponde a un grado 0; la presencia de lesiones focales no confluentes, a un grado 1; las lesiones inicialmente confluentes, a un grado 2; y la afectación difusa confluente, a un grado 3.
A partir de esta escala, se ha tratado de delimitar la «normalidad» (atribuible al envejecimiento) de la afección, de manera que se considera el grado 1 normal con el envejecimiento, el grado 2 patológico en menores de 75 años y el grado 3 patológico en todos los casos.
Imágenes puntiformes hiperintensas «anormales» en la sustancia blanca
Cuando la presencia de IPHSB es patológica, puede traducir una afección adquirida o hereditaria. Dentro de las afecciones adquiridas de la sustancia blanca, la causa hipóxico-isquémica microvascular es, con mucho, la más frecuente, ya sea aterotrombótica, por factores de riesgo cerebrovascular (FRCV), o embolígena.
Debe considerarse siempre en primer lugar, aún en ausencia de FRCV típicos, a no ser que existan indicios clínicos y analíticos que hagan pensar en otra etiología. La esclerosis múltiple (EM) es la segunda causa en frecuencia, seguida de lejos por la vasculitis, las infecciones, las intoxicaciones o los traumatismos, entre otras causas.
En cuanto a la afección hereditaria, las leucodistrofias constituyen un grupo de enfermedades consideradas raras que, aunque suelen aparecer en la edad pediátrica, pueden debutar en el adulto. Estas enfermedades metabólicas suelen afectar a la sustancia blanca de forma bastante simétrica y extensa (no puntiforme), y suelen dañar el tronco encefálico y el cerebelo, con la excepción de las enfermedades mitocondriales, que muestran lesiones más asimétricas y suelen afectar a la sustancia gris.
Fisiopatología básica
Un posible mecanismo de lesión de la sustancia blanca es la afectación primaria de una arteriola o vénula cerebral. Ésta compromete la irrigación del parénquima que depende de ellas y produce una lesión. La afectación de la sustancia blanca por enfermedad microvascular comprende un gran espectro de patología: hipoxia-isquemia, inflamación granulomatosa o no granulomatosa, infección, enfermedad por depósito de sustancias, tóxicos, enfermedades metabólicas, traumatismos, etc.
Otro posible mecanismo fisiopatológico de la leucoencefalopatía es una infiltración celular o un acúmulo de sustancias patológicas en el espacio perivascular que también se puede manifestar radiológicamente como lesiones focales en la sustancia blanca. Su causa suele ser inflamatoria no infecciosa (como en el caso de la EM u otras enfermedades desmielinizantes, de algunas vasculitis o de algunas enfermedades granulomatosas), infecciosa atípica (enfermedad de Lyme, criptococosis, cisticercosis parenquimatosa), metabólica (mucopolisacaridosis) o traumática (lesión axonal difusa).
Ambos procesos fisiopatológicos pueden coexistir en una misma enfermedad.
Teniendo en cuenta la anatomía de la microcirculación cerebral y la de su intersticio, se puede abordar la afección de la sustancia blanca considerando qué elementos se hallan más afectados en los diferentes grupos de leucoencefalopatías. En este sentido, trataremos de aproximarnos a la fisiopatología de la enfermedad que condiciona las IPHSB a partir de la identificación de un patrón semiológico predominante.
Considerando varios elementos semiológicos definiremos tres grandes patrones:
- Patrón vascular (PV) o microvascular, que suele ser debido a una lesión arteriolar. Es el más prevalente.
- Patrón perivascular (PpV), que suele ser debido a una inflamación perivascular, entre otras causas menos frecuentes. El paradigma de este patrón es la EM, en la que se ha descrito una inflamación perivenular de origen autoinmune que ocasiona la desmielinización.
- Patrón inespecífico (PI), en los casos en que no identificamos ninguno de los dos anteriores, y que suele ser debido a enfermedad microvascular.
Elementos semiológicos en las imágenes puntiformes hiperintensas de la sustancia blanca
Para el abordaje radiológico de un caso de IPHSB los elementos semiológicos básicos a analizar son su distribución y localización, la forma, el tamaño, el realce tras la administración de contraste, la presencia de hemorragia o microhemorragia y la afectación de la sustancia gris. La descripción de cada uno de estos elementos nos puede ayudar a identificar uno de los tres patrones semiológicos propuestos, de manera que nos facilitará un diagnóstico diferencial adecuado en cada caso.
Distribución y localización
Las IPHSB pueden aparecer con una distribución preferentemente supratentorial, infratentorial o tanto supra como infratentorial. En general la presencia de lesiones de distribución fundamentalmente supratentorial nos sugerirá en primer lugar que nos encontramos ante una enfermedad de pequeño vaso y, por tanto, favorecerá un PV. El hecho de que además la distribución preferentemente frontoparietal reforzará esta sospecha.
Dentro de la distribución supratentorial se pueden definir 4 grandes áreas: subcortical, periventricular, profunda o en el cuerpo calloso.
Microinfartos cerebrales
Los microinfartos cerebrales son pequeñas lesiones vasculares en el cerebro y su acumulación puede conllevar una disminución de las capacidades cognitivas, incluso ser causa de demencia o contribuir al desarrollo del Alzheimer.
La prevención y detección temprana de la presencia de microinfartos cerebrales es clave para minimizar su impacto en la autonomía de la persona y favorecer su calidad de vida. Los microinfartos cerebrales son minúsculas lesiones vasculares de tamaño variable (alrededor de 0,05 a 3 milímetros de diámetro) y silentes (es decir, que van apareciendo sin dar síntomas), que por lo general son de origen isquémico.
Individualmente, las lesiones son microscópicas y silentes. Sin embargo, la acumulación de muchos microinfartos cerebrales a lo largo del tiempo puede llegar a asociarse a síntomas como déficits cognitivos o motores.
Gracias a la investigación sabemos, por un lado, que el área afectada por un microinfarto puede llegar a ser hasta 12 veces mayor que el núcleo visible de la lesión y, por otro lado, que sus efectos son prolongados en el tiempo, ya que la alteración del flujo sanguíneo en el área afectada puede durar semanas.
Las personas que padecen enfermedades cerebrovasculares y demencia vascular presentan una mayor incidencia de microinfartos cerebrales en comparación a personas con la enfermedad de Alzheimer.
La magnitud del daño y la localización de estas lesiones en el cerebro están muy relacionada con las capacidades del procesamiento de la información y que pueden verse afectadas y con la sintomatología que se manifiesta.
La localización y concentración de los microinfartos en las distintas áreas cerebrales da lugar a distintos tipos de afectación. En líneas generales, lesiones en áreas anteriores del cerebro se suelen relacionar con déficits relacionados con el razonamiento, la capacidad de planificación y de resolución de problemas y con algunos cambios conductuales, como puede ser una acusada apatía o tendencia a actuar de forma desinhibida.
Los microinfartos responden a múltiples causas de origen vascular que pueden coexistir en una misma persona. Todas estas alteraciones pueden provocar la isquemia o infarto de pequeños territorios cerebrales irrigados por arterias y arteriolas de pequeño calibre.
Angiopatía amiloide
Es frecuente que las personas con enfermedad de Alzheimer también tengan patologías vasculares en su cerebro. La angiopatía amiloide se caracteriza por la concentración de proteína amiloide en las paredes de las arterias de pequeño calibre que irrigan el córtex. También puede asociarse a la presencia de microsangrados.
Estos resultados sugieren que la combinación de patología vascular y de enfermedad de Alzheimer da lugar a efectos sinérgicos, es decir, que se potencian entre sí, produciendo un impacto mayor que el que esperaríamos simplemente al sumar el riesgo asociado a cada condición por separado.
Factores de riesgo
Entre estos factores de riesgo destacan la hipertensión arterial, la diabetes y el colesterol elevado, así como ciertos hábitos tóxicos como el consumo de tabaco y consumo excesivo de alcohol.
También forma parte de este plan de prevención el realizar un control médico regular sobre los factores riesgo cardiovascular, y mantener una buena adherencia al tratamiento médico pautado.
Demencia vascular
La demencia vascular (DV) hace referencia al deterioro cognitivo global originado a través de la existencia de enfermedad vascular cerebral de tipo isquémico o hemorrágico, siendo necesario un nexo temporal entre ambas condiciones.
Los principales factores de riesgo para el desarrollo de patología vascular cerebral son bien conocidos, como la edad avanzada, la hipertensión arterial (HTA), la diabetes mellitus, las dislipidemias, el tabaquismo, el alcohol y la fibrilación auricular.
Los infartos lacunares son lesiones cavitadas de entre 1 y 20 mm de diámetro producidas por la oclusión de arterias perforantes o por el desarrollo de pequeñas hemorragias. Son subcorticales y predominan en los ganglios basales, tálamo, protuberancia o sustancia blanca hemisférica.
En la denominada encefalopatia arteriosclerótica subcortical o encefalopatía de Binswanger se encuentra rarefacción y desmielinización isquémica de la sustancia blanca de los centros semiovales, generalmente asociada a otros hallazgos relacionados con patología de pequeños vasos (lipo-hialinosis, fibro-hialinosis). Representa la afectación vascular crónica de la sustancia blanca a través de procesos como la hipertensión arterial.
Tipos de demencia vascular
La demencia vascular cortical se origina a través de infartos corticales o córticosubcorticales de origen trombótico, embólico o hemodinámico. Son infartos en territorios de arterias de mediano o gran calibre y se encuentran déficit en el área del lenguaje, de la praxis, del cálculo, de las funciones visuoespaciales y de la memoria. Se añaden alteraciones de la conducta o psicológicas y el curso clínico suele ser escalonado.
La demencia vascular subcortical surge a partir de una afectación de pequeños vasos por HTA, diabetes, angiopatía amiloide, angiopatías hereditarias, etc. Su curso clínico puede ser insidioso sin evidencia de ictus en su evolución, planteando dificultades diagnósticas con otras demencias de origen degenerativo como el alzhéimer. En los estudios neuropsicológicos los rasgos más significativos son las alteraciones de la función ejecutiva, de la evocación de la memoria, los trastornos de la atención y de la concentración, la apatía y los cambios afectivos.
Diagnóstico de la demencia vascular
El diagnóstico de demencia vascular lleva implícita la existencia de enfermedad vascular cerebral, haya sido ésta sintomática o no a través de ictus previos.
El EEG mostrará con mayor probabilidad áreas de sufrimiento focal en la demencia vascular con respecto a la enfermedad de Alzheimer, pero su validez discriminativa es escasa ante un paciente concreto.
Tratamiento de la demencia vascular
El tratamiento de los síntomas cognitivos se centra en el uso de agentes farmacológicos que potencien la transmisión colinérgica en las áreas en donde ésta resulta deficitaria. Los inhibidores de la colinesterasa que han demostrado su eficacia en la enfermedad de Alzheimer son objeto de numerosos estudios que parecen también refrendar su uso en la demencia vascular.
Enfermedad de Alzheimer
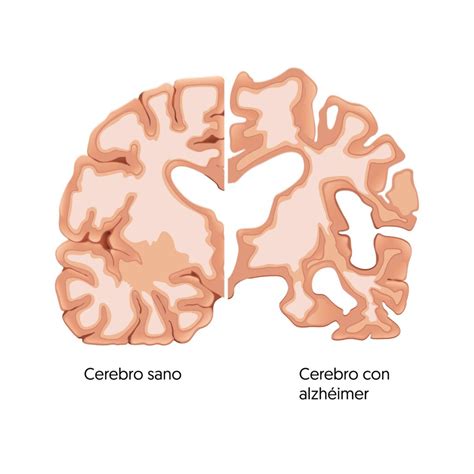
La enfermedad de Alzheimer es la causa más común de demencia y representa un gran desafío para las personas que la padecen, y para quienes las acompañan en ese camino. Esta enfermedad neurodegenerativa afecta el cerebro de una persona con Alzheimer de manera progresiva, alterando su estructura y funciones.
En el cerebro de una persona con Alzheimer, se producen alteraciones diversas que van progresando. Los cambios más precoces que se producen, y que resultan fundamentales para el daño cerebral, son dos: la acumulación de algunas proteínas tóxicas, que dañan y destruyen neuronas, y la neuroinflamación crónica, que agrava este daño.
Fases de la enfermedad de Alzheimer
Según la Escala Global del Deterioro (GDS), la enfermedad de Alzheimer se desarrolla en siete fases. Sin embargo, cada paciente es un mundo, y no en todos evolucionará de la misma manera. Conocer cómo puede ser este proceso ayudará a la persona a tomar decisiones que afectarán a su cuidado.
- Etapa 1: La persona está mentalmente sana.
- Etapa 2: La persona se queja de que tiene algunas dificultades cognitivas y funcionales (deterioro cognitivo subjetivo).
- Etapa 3: La persona manifiesta déficits sutiles que son percibidos por los que se encuentran en su entorno más próximo (deterioro cognitivo leve).
- Fase del alzhéimer 4: Los problemas del paciente suelen ser más evidentes a la hora de realizar actividades instrumentales.
Las etapas de 1-3 constituyen las fases previas a la demencia y de la 4 a la 7, el paciente ya ha desarrollado alzhéimer.
Demencia frontotemporal (DFT)
La demencia frontotemporal (DFT) conforma un grupo de desórdenes neurodegenerativos heterogéneos clínica y neuropatológicamente. Se caracteriza por cambios en el comportamiento social, en la personalidad y por afasia, acompañados de la degeneración de los lóbulos temporal o frontal.
Según lo descrito por la literatura, la DFT es una de las causas más comunes de demencia en edades tempranas, con una media que oscila entre 45 y 64 años. En nuestro caso, observamos un tipo de DFT variante conductual (VC), que representa el 50 % de todos los casos. Los puntos clave en el diagnóstico de esta entidad son los cambios progresivos en la personalidad y en el comportamiento.
A este respecto hay que destacar que este grupo de pacientes suele desarrollar desinhibición o comportamiento social inapropiado. La apatía es otra de las manifestaciones; se ha descrito incluso que algunos pacientes pueden participar menos en las conversaciones, lo cual es muchas veces confundido con depresión.
| Condición | Características |
|---|---|
| Demencia Vascular | Deterioro cognitivo debido a enfermedad vascular cerebral (isquémica o hemorrágica). |
| Enfermedad de Alzheimer | Enfermedad neurodegenerativa progresiva que afecta la memoria, el pensamiento y el comportamiento. |
| Demencia Frontotemporal | Grupo de desórdenes neurodegenerativos caracterizados por cambios en la personalidad, comportamiento y afasia. |