La histología trata el estudio de los tejidos biológicos a un nivel más complejo y detallado que la citología. Mientras que la citología se centra en las células individuales, la histología examina cómo estas células se organizan en tejidos y cómo esos tejidos forman órganos y sistemas en el cuerpo.
El motivo es que permiten a los profesionales veterinarios ver más allá de los síntomas superficiales y comprender las raíces de las condiciones médicas. Al trabajar de cerca con veterinarios en la preparación y análisis de muestras, los auxiliares con conocimientos en estas áreas son capaces de facilitar diagnósticos rápidos y precisos.

Citología vs. Histología
La citología es una rama de la biología que se enfoca en examinar células individuales extraídas de tejidos. Cuando un veterinario sospecha de una enfermedad, una de las primeras acciones puede ser realizar una citología. Esto implica tomar una pequeña muestra de células del animal, ya sea mediante un raspado de piel, una punción con aguja fina de un tumor o una aspiración de un líquido corporal.
El análisis de estas células permite identificar características anormales, como la forma y tamaño irregular de las células, la presencia de múltiples núcleos, o cambios en la estructura que pueden indicar una enfermedad específica.
Pongamos un ejemplo. Supongamos que un perro presenta un bulto sospechoso. La citología puede determinar rápidamente si el bulto es benigno, como un lipoma (un tumor graso común y no canceroso), o si muestra signos de cáncer, lo que requiere intervención médica inmediata.
Uno de los ejemplos más comunes de la aplicación de la citología es el examen rápido de las orejas de un perro para detectar infecciones por hongos o bacterias.
El Proceso de Preparación de Muestras Histológicas
El primer paso en el estudio histológico es la preparación de la muestra, que requiere precisión y cuidado. Este proceso comienza con la fijación del tejido, que implica preservar las muestras de tejido en una solución química para evitar su deterioro.
Una vez que las muestras están preparadas y teñidas, se examinan bajo el microscopio. Este examen puede revelar mucho sobre la salud del animal. Además, la histología es indispensable en el diagnóstico de cánceres.
En cuanto a la histología, un caso destacado es el estudio de biopsias de tumores. La capacidad de diferenciar entre tumores benignos y malignos mediante técnicas histológicas es invaluable.
También hay que tener en cuenta que las técnicas de citología e histología requieren herramientas específicas. En el día a día, los auxiliares utilizan microscopios, colorantes especiales y equipos de corte de tejidos para preparar y analizar las muestras.
Biopsias, muestras grandes o grasosas; tejidos diferentes necesitan tratamientos diferentes. Por eso, cada tipo y tamaño de tejido tiene el tratamiento que se merece.
El proceso de tinción y cubreobjetos totalmente automatizado y de alto rendimiento, optimiza la preparación de muestras con características avanzadas de automatización que minimizan el manejo manual.
El sistema modular especular para efectuar la inclusión en parafina de muestras histológicas, ha sido concebido con tecnologías avanzadas y dotado de características únicas, garantiza la máxima seguridad para el operador y un nuevo nivel de estandarización de las muestras.
El AP32 IF ELITE es un sistema innovador capaz de procesar 32 portaobjetos IFA (40 portaobjetos opcionales). Nuestra experiencia en el desarrollo de sistemas de tinción de portaobjetos se remonta a 1956, cuando se introdujo en los laboratorios el primer sistema Hematek.
VIDEHISTO #02 | Fundamentos de la tinción en histología
Métodos de Fijación de Tejidos
Existen diferentes formas de fijar los tejidos dependiendo del tipo de fijador, de la estructura a fijar y de lo que queramos observar.
Fijadores Físicos
Los fijadores físicos se basan bien en una congelación muy rápida del tejido o bien en la aplicación de calor elevado. La congelación rápida es un buen método de preservación de las características moleculares, puesto que no se verán alteradas por ninguna sustancia química.
La congelación es conveniente que sea rápida puesto que así se impide la formación de grandes cristales de hielo que nos destrozarían la estructura del tejido. Por ello es conveniente no usar piezas mayores a 2 mm para que no se retarde la congelación de las zonas centrales de la pieza.
Una congelación rápida se consigue sumergiendo la pieza en isopentano (-170 ºC) enfriado con nitrógeno líquido (-196 ºC), o colocando la muestra sobre un metal, el cual se sumerge parcialmente en nitrógeno líquido, en mezclas de hielo seco y acetona (-70 ºC) o incluso en helio líquido (-268 ºC).
Asimismo, cuando sea posible, es conveniente embeber la muestra en anticongelantes, también llamados crioprotectores. La crioprotección es siempre recomendable, aunque no siempre es posible. Normalmente se emplean como agentes crioprotectores al dimetilsulfóxido, el glicerol y la sacarosa, bien solos o mezclados en diferentes concentraciones.
Hay que tener en cuenta, sin embargo, que una vez que el tejido se haya cortado se vuelve a descongelar y hay que protegerlo de los procesos de degradación. Existen variantes a la técnica de congelación como son la criodesecación o liofilización y la criosustitución.
La criodesecación parte de tejido previamente congelado al que posteriormente se le sublima el hielo, es decir, el agua pasa de estado sólido a gaseoso sin pasar por estado líquido. Al eliminar el agua se impide que se den reacciones químicas, por lo que, además de la fijación, este método preserva el tejido en el tiempo.
La criosustitución también parte de tejido congelado pero en este caso se produce una sustitución lenta del hielo por una solución fijadora.
La fijación por calor no es frecuente en histología, puesto que produce deterioros de los tejidos. Su efecto es la coagulación de proteínas y disolución de lípidos. Sin embargo, se emplea para la observación de microorganismos, ya que preserva la forma de éstos y sirve para su identificación.
Hoy en día, sin embargo, se suele emplear el calor como un complemento a la fijación química. Así, las muestras inmersas en un fijador se introducen en un microondas y se llevan hasta temperaturas de unos 55 ºC. Esta temperatura no produce artefactos y tiene dos ventajas: incrementa la velocidad de fijación y reduce el tiempo fijación desde varias horas o días a decenas de minutos.
El uso del microondas permite que el calor sea homogéneo en toda la muestra de forma inmediata (si se hiciera en un baño caliente habría un gradiente de calor en la muestra desde la parte externa a la más interna). Se cree que el incremento de la velocidad de fijación se debe sólo al calor generado y no al efecto directo de las microondas.
Fijadores Químicos
Los métodos químicos utilizan soluciones acuosas compuestas por moléculas fijadoras que establecen puentes entre las moléculas del tejido, manteniéndolas en sus lugares originales e impidiendo su degradación. Hay que considerar que los fijadores químicos afectan en mayor o menor medida al tejido, tanto física como químicamente. Los efectos físicos suelen ser retracciones o distensiones, y la mayoría endurecen el tejido.
Hay dos métodos básicos de fijación con fijadores químicos: inmersión y perfusión. En el método de inmersión las piezas de tejido se sumergen en la solución fijadora (Figura 1). En algunos casos se necesitan fijar extensiones de sangre o cortes por congelación sin fijación previa. En estos casos siempre se fijan por inmersión en la sustancia fijadora.

Las piezas de tejido no deberían superar los 0.5 cm de espesor para que el fijador alcance el interior de la pieza antes de que ésta comience a deteriorarse. La velocidad de penetración del fijador depende de cada fijador y de las características del tejido. Esta velocidad nos condicionará el tamaño de la muestra. Para fijadores lentos se recomiendan piezas de 0.2 cm de tamaño. Esto también se ve afectado por el tipo de tejido.
El tiempo de fijación, para una mismo tipo de muestra, depende de cada tipo de fijador: velocidad de difusión y velocidad de fijación (la rapidez e intensidad con la que establece puentes o coagula proteínas). Debe ser suficiente para que la muestra quede bien fijada pero no excesivo para evitar deterioros o alteraciones del tejido.
Una agitación suave durante la fijación ayuda a la penetración del fijador y disminuye el tiempo.
Por este procedimiento la solución fijadora se introduce a través del sistema circulatorio por el cual accede a todas las células del tejido gracias a la red de capilares (Figura 2). Mediante este método se puede fijar un animal completo introduciendo la solución fijadora a través del ventrículo izquierdo del corazón.
El fijador llegará a todas las células irrigadas por por el sistema circulatorio (circuito corporal) y bombeado por una bomba peristáltica. Si se quieren fijar los pulmones habría que introducir el fijador por el ventrículo derecho. También podemos fijar un único órgano en el caso de que podamos introducir la solución fijadora en la arteria principal que irriga dicho órgano (Figura 3). La perfusión no siempre es posible como en la mayoría de las biopsias o en los tejidos vegetales.
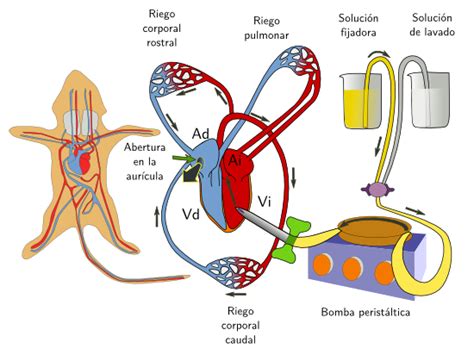
El método de fijación por perfusión es mucho más efectivo que el de inmersión ya que la solución fijadora llega rápidamente a escasa distancia de todas las células de la estructura perfundida.
Antes de introducir el fijador en el sistema de vasos sanguíneos hay que eliminar previamente la sangre con una solución de lavado oxigenada, ya que de otra manera su interacción con el fijador produce trombos que impedirían la fijación de determinadas zonas del animal o del órgano.
Este método de fijación por perfusión requiere conocer la presión a la que se va a introducir la solución fijadora en el animal o estructura, la cual debe ser similar a la que posee la presión sanguínea normal en estado vivo. La presión que ejercerá la solución fijadora se puede regular mediante bombas peristálticas (Figuras 2 y 3) o por gravedad, es decir, variando la altura a la cual se coloca la solución fijadora respecto a la del animal.
Inmunohistoquímica (IHC): Fundamentos y Aplicaciones
La inmunohistoquímica (IHC) es una técnica utilizada en las ciencias biomédicas para la detección de antígenos específicos en las células de una sección de tejido, explotando el principio de anticuerpos uniendo a antígenos en sitios biológicos. El uso de la IHC se ha extendido significativamente debido a su capacidad para proporcionar visualizaciones precisas de la distribución y localización de proteínas específicas dentro de diferentes partes de tejidos biológicos.
El proceso comienza con la preparación de la muestra, que típicamente involucra la inclusión de tejido en parafina para preservar la arquitectura del tejido. Luego, los cortes finos del tejido se montan en diapositivas para el análisis. Antes de aplicar los anticuerpos, las secciones de tejido requieren desparafinización y rehidratación.
Posteriormente, para mejorar la visualización de los antígenos, las secciones pueden ser sometidas a tratamiento de recuperación del antígeno, generalmente mediante calor o tratamiento enzimático. Los anticuerpos primarios especificos son aplicados a la sección de tejido, donde se vinculan con el antígeno diana.
Esta unión es luego detectada por un anticuerpo secundario que está conjugado con un marcador, como una enzima o un fluorocromo, lo que permite la visualización mediante una reacción cromogénica o fluorescente. El resultado es que los antígenos diana en la sección de tejido pueden ser visualizados bajo un microscopio, típicamente como señales de color en el contexto de la estructura del tejido.
Esta técnica es particularmente importante, ya que permite la localización molecular y celular precisa de antígenos, lo que es crítico para la investigación y diagnóstico en histología, patología y otras áreas biomédicas. El análisis detallado proporcionado por la IHC ayuda a comprender mejor la patogénesis de las enfermedades y también en la identificación de posibles objetivos terapéuticos.
Preparación de Muestras y Técnicas en Inmunohistoquímica
La preparación de muestras en inmunohistoquímica es un proceso crítico que requiere precisión y cuidado, ya que la calidad de la muestra determina en gran medida la fiabilidad de los resultados obtenidos. Este proceso comienza con la recolección del tejido, que debe ser manipulado lo menos posible para evitar la degradación de los antígenos.
El fijador más comúnmente usado es el formaldehído, que ayuda a preservar la estructura de los tejidos y antígenos, aunque la elección del fijador puede variar dependiendo del tipo de tejido y los antígenos de interés.
Una vez fijada, la muestra se deshidrata a través de una serie de baños con alcoholes de concentraciones ascendentes y luego se aclara en xileno. Este paso es crucial para preparar la muestra para la inclusión en parafina, lo que facilitará el corte de secciones delgadas de tejido. Las secciones típicamente tienen un grosor de 4 a 5 micrómetros y se montan en portaobjetos tratados para aumentar la adhesión del tejido.
El proceso de recuperación antigénica sigue a la desparafinización y rehidratación de las secciones de tejido, usualmente usando soluciones calientes de citrato de sodio o Tris-EDTA. Este paso es fundamental para desenmascarar los epítopos que han sido ocultados durante el proceso de fijación. La elección del método de recuperación antigénica dependerá del anticuerpo específico y del antígeno que se está estudiando.
Finalmente, se bloquean los sitios de unión inespecíficos en el tejido para prevenir el marcado no específico. Esto se logra incubando la muestra con sueros o soluciones bloqueadoras que contienen proteínas como el suero bovino o la caseína. Tras el bloqueo, la muestra está lista para la aplicación de los anticuerpos primarios y secundarios, que serán los responsables de identificar y señalizar la presencia de los antígenos de interés.
Los anticuerpos pueden ser monoclonales o policlonales. Los monoclonales son específicos para un solo epítopo de un antígeno, ofreciendo alta especificidad y consistencia, mientras que los policlonales se unen a múltiples epítopos, proporcionando una señal más fuerte, pero con mayor riesgo de reactividad cruzada.
Uno de los marcadores más comunes es la proteína tumoral p53, utilizada en el diagnóstico de numerosos tipos de cáncer. Los anticuerpos contra p53 pueden ayudar a identificar la sobreexpresión de esta proteína, un indicativo de la posible presencia de tumor maligno. Otro marcador importante es el CD20, utilizado para identificar linfomas B. Los anticuerpos contra CD20 son efectivos para diagnosticar y evaluar el tratamiento en pacientes con este tipo de cáncer.
En neurociencia, se utilizan anticuerpos contra la proteína tau y amiloide-beta para la investigación y diagnóstico de enfermedades neurodegenerativas como el Alzheimer. Estos anticuerpos permiten visualizar los depósitos de estas proteínas en el cerebro, facilitando el estudio de la patología y la progresión de la enfermedad.
Con el avance de la tecnología, también hemos visto el desarrollo de anticuerpos conjugado a enzimas, fluoróforos, o biotina que permiten una mayor facilidad en la detección y cuantificación de los antígenos. Estos anticuerpos conjugados son cruciales en técnicas automatizadas de inmunohistoquímica, mejorando la eficiencia y precisión del análisis histológico.
Aplicaciones Clínicas de la Inmunohistoquímica
La inmunohistoquímica (IHC) posee un papel fundamental en numerosas aplicaciones clínicas, siendo una herramienta esencial en el diagnóstico patológico, la determinación del pronóstico y el desarrollo de estrategias terapéuticas para diversas enfermedades. Una de sus aplicaciones más destacadas es en la oncología, donde la IHC ayuda a caracterizar los tipos de células cancerosas, identificando la expresión de marcadores tumorales específicos que pueden influir en la elección de terapias dirigidas.
Por ejemplo, en el cáncer de mama, la IHC se utiliza para detectar receptores de estrógeno y progesterona, así como la sobreexpresión del HER2/neu, un receptor que promueve el crecimiento del tumor. La presencia o ausencia de estos marcadores guía la selección de tratamientos hormonales o terapias dirigidas como el trastuzumab en pacientes con HER2 positivo.
En el ámbito neurológico, la técnica permite identificar proteínas patogénicas, como la proteína tau y beta-amiloide en pacientes con Alzheimer, proporcionando una vía para el diagnóstico definitivo de la enfermedad. Asimismo, en trastornos inflamatorios y autoinmunes, la IHC es empleada para detectar marcadores inflamatorios y autoanticuerpos que contribuyen a la patología de condiciones como la artritis reumatoide y lupus eritematoso sistémico.
Además, la IHC es utilizada en la investigación clínica para el desarrollo y validación de nuevos biomarcadores y tratamientos. Por ejemplo, se está explorando su uso en la identificación de marcadores de respuesta a inmunoterapias en diferentes tipos de cáncer, facilitando así una medicina más personalizada y efectiva.
Estas aplicaciones reflejan cómo la IHC no solo contribuye al manejo clínico actual, sino que también impulsa avances significativos en la medicina personalizada y de precisión, asegurando tratamientos más eficaces y adaptados a las características moleculares individuales de cada paciente.
Desafíos y Desarrollos Futuros en Inmunohistoquímica
Uno de los desafíos principales en la inmunohistoquímica es la estandarización de protocolos a nivel global. Actualmente, la variabilidad en los procesos de preparación de muestras y en la aplicación de anticuerpos puede llevar a resultados inconsistentes, lo cual es crítico, especialmente en contextos clínicos donde se utilizan estos resultados para tomar decisiones terapéuticas precisas. La adopción de normas internacionales y el desarrollo de controles de calidad más rigurosos son necesarios para aumentar la fiabilidad de los diagnósticos basados en esta técnica.
Paralelamente, el avance en el desarrollo de nuevos biomarcadores está expandiendo las capacidades diagnósticas y pronósticas de la inmunohistoquímica. El desafío aquí se centra en la validación clínica de estos marcadores y en su integración efectiva en los paneles de pruebas estándar. Este proceso requiere estudios extensos y colaboración entre investigadores, clínicos y entidades reguladoras para asegurar que los nuevos marcadores sean tanto específicos como sensibles.
Además, la evolución de la tecnología digital y la inteligencia artificial presenta una oportunidad prometedora para el futuro de la inmunohistoquímica. El desarrollo de software avanzado que pueda analizar imágenes y proporcionar diagnósticos precisos podría transformar la práctica de patología, reduciendo la carga de trabajo manual y mejorando la precisión de los diagnósticos. Ya se están realizando investigaciones en este ámbito, y los primeros resultados son prometedores, aunque la integración de estas tecnologías en la práctica clínica diaria aún enfrenta barreras significativas, incluyendo la necesidad de extensas validaciones y aprobaciones regulatorias.
Finalmente, el desafío de mantener la calidad y la disponibilidad de reactivos específicos, principalmente anticuerpos monoclonales, sigue siendo relevante. La producción de estos reactivos es compleja y su calidad puede variar, afectando la reproducibilidad de los resultados. Las innovaciones en tecnologías de producción y purificación de anticuerpos, así como mejoras en la logística de suministro, son cruciales para superar estas limitaciones.
Equipos y Sistemas Automatizados
Para facilitar el proceso de preparación de muestras y mejorar la eficiencia en los laboratorios, se han desarrollado diversos equipos y sistemas automatizados. Algunos de estos incluyen:
- Sistema CellMek SPS: Automatiza el flujo de trabajo de preparación de muestras de citometría de flujo de principio a fin sin intervención del usuario.
- Plataforma Centri® de Markes International: Ofrece muestreo desatendido de alta sensibilidad y preconcentración de COV y COVV en muestras líquidas, sólidas y gaseosas.
- Akribis-Air: Un sistema inteligente e independiente de preparación de muestras que ofrece lo último en innovaciones de procesamiento y es una máquina independiente altamente automatizada.
- Micromeritics FlowPrep: Aplica una combinación de calor y una corriente de gas inerte a la muestra.
Recomendación personal de marcas
La inmunohistoquímica es una herramienta indispensable en el diagnóstico y la investigación biomédica, aunque enfrenta desafíos como la estandarización de protocolos y la mejora en la especificidad y sensibilidad de los anticuerpos. Afortunadamente, el futuro parece prometedor, gracias a los avances en tecnología y la contribución de varias compañías líderes en el sector.
- Antibodies.com: Ofrece una amplia gama de anticuerpos de alta calidad, que son esenciales para la precisión en los resultados de inmunohistoquímica. Sus productos son validados rigurosamente, asegurando su eficacia en aplicaciones de diagnóstico y de investigación.
- ELK Biotech: Destaca por su innovación en el desarrollo de reactivos para inmunohistoquímica, proporcionando soluciones avanzadas que mejoran la visualización de proteínas y estructuras celulares en tejidos complejos.
tags: #encia #corte #histologico