La mandíbula es la estructura ósea del maxilar inferior y de la parte inferior de la cara. Es el mayor y más fuerte de los huesos de la cara y proporciona encajes para mantener los dientes inferiores en su sitio. La mandíbula forma la parte inferior del cráneo y consta de dos partes: una parte horizontal llamada cuerpo, y dos partes verticales llamadas ramas que ascienden casi verticalmente desde la parte posterior del cuerpo mandibular.
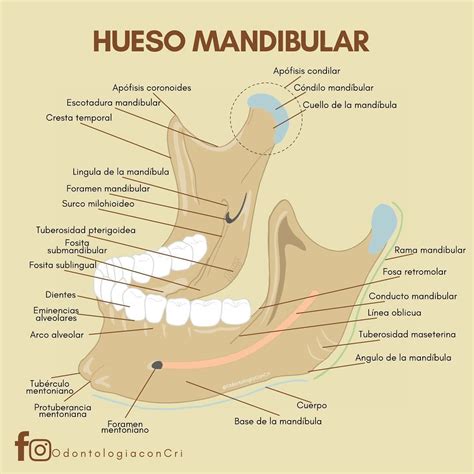
Anatomía de la mandíbula.
Mecanobiología de los Huesos Maxilares
La mecanobiología estudia la interacción entre las señales mecánicas y los procesos biológicos que se producen en las células y tejidos. La carga mecánica puede influir en la proliferación, diferenciación y metabolismo celular, por lo que tiene un papel crucial en el crecimiento, adaptación, regeneración y bioingeniería de los tejidos vivos.
Desde el punto de vista biomecánico, ningún tejido vivo puede compararse a otro material de ingeniería, ya que dichos tejidos presentan un continuo proceso de regeneración y remodelación que permite mejorar su estructura en función de los esfuerzos a los que es sometido (1). Van der Meulen describió la mecanobiología esquelética como "la ciencia que estudia las fuerzas mecánicas que modulan la morfología y la adaptación estructural de los tejidos esqueléticos; es decir, hueso, cartílago, ligamento y tendón" (2).
Existen tres aspectos que han hecho avanzar enormemente la mecanobiología ósea en los últimos años:
- Los modelos informáticos de estructuras que permiten el análisis del efecto de fuerzas físicas en las complejas geometrías del hueso.
- La biología molecular que permite detectar la expresión de genes y la síntesis de proteínas tras la aplicación de diferentes fuerzas mecánicas.
- El avance de la tecnología de imagen, que permite identificar las características micro y nanoestructurales del tejido.
En este artículo se revisan los conceptos generales que se estudian en la mecanobiología y biomecánica de los hueso maxilares. Se establecen las principales propiedades biomecánicas del hueso en las diferentes escalas de medición y determinados factores que influyen en la reacción del hueso perimplantario ante las cargas biomecánicas.
Propiedades Biomecánicas del Hueso (Nivel Macro, Micro y Nanométrico)
Hay que tener en cuenta que durante varios años se han establecido las propiedades biomecánicas del hueso basándose únicamente en la escala macrométrica (escala de centímetros o milímetros), valorando las diferencias estructurales visibles a simple vista que existen entre el hueso trabecular y el hueso cortical (Fig 2). Sin embargo, hoy en día se puede estudiar la estructura del hueso a nivel orgánico, tisular, celular o molecular (10). Las aproximaciones micro y nanoestructurales al hueso están reflejando las diferentes propiedades biomecánicas de los distintos tipos de tejido óseo que se pueden incluir tanto en el hueso trabecular como en el cortical, es decir el hueso reticular, el hueso de fibras paralelas y el hueso laminar.
De manera general, en el hueso, la resistencia (resistencia a la deformación) y la rigidez lo aporta la fase inorgánica, mientras que la tenacidad (resistencia a la fractura) lo aporta la fase orgánica (11).
Nivel Macro y Micrométrico (Órgano/Tejido/Célula)
Teniendo en cuenta el carácter general anisotrópico no homogéneo del hueso, el hueso cortical se suele evaluar estructuralmente de manera imprecisa como un material isotrópico (con la misma propiedad biomecánica al ser medida en cualquier dirección), mientras que el hueso trabecular presenta mayor grado de anisotropía en función de las cargas que haya recibido en cada zona (1). Si las propiedades son diferentes en las tres direcciones del espacio se habla de material ortotrópico, mientras que sin las propiedades son iguales en dos direcciones, se habla de isotropía transversal (12).
Las propiedades biomecánicas son variables entre el hueso cortical y trabecular principalmente porque el espacio poroso en el primero es del 5-10% mientras que en el segundo se encuentra entre 30-90% (10). La morfología general del hueso, le permite tener una estructura rígida y ligera a la vez, ya que el hueso cortical facilita la rigidez mientras que las trabéculas internas minimizan el peso (1).
De manera general, las propiedades biomecánicas del hueso van a depender de su contenido acuoso, de la porosidad (densidad) y del contenido mineral (1).
Hueso Cortical
Los valores obtenidos para el hueso cortical son menos dispersos que los encontrados en el hueso trabecular. En general, el módulo de elasticidad se encuentra entre 15-20 GPa (13) la resistencia a la tensión se encuentra entre los 80-150 Mpa, y la resistencia a la compresión entre los 90-280 Mpa, debido principalmente al carácter anisotrópico del hueso (1). Se ha observado que la cortical mandibular es anisotrópica, de tal forma que al igual que la diáfisis femoral, es mas rígida en la dirección longitudinal que en la radial o tangencial, teniendo en estas direcciones un 40-80% del valor de rigidez que tiene en la dirección longitudinal. La resistencia a la compresión es de 200, 110 y 100 Mpa en la dirección longitudinal, tangencial y radial respectivamente (14).
Por otro lado hay que considerar que los valores de resistencia del hueso cortical son variables en función de la edad. De esta manera la resistencia a la tensión máxima desciende desde los 120 Mpa con 30 años a 70 Mpa a los 100, mientras que el límite máximo de deformación cae del 3,3% a los 30 años al 1% a los 100 años. De la misma manera se observan similares efectos en el hueso trabecular (15). Se ha observado en hueso cortical femoral que a partir de los 35 años hay una disminución por década del módulo elástico de 0,35 GPa, de resistencia a la flexión de 6,25 Mpa, y de energía de fractura (tenacidad) de 0,03 Kj/m2. El tamaño de las microgrietas también se ha observado aumentado con la edad con valores de 500 µm a los 35 años y de hasta 1 mm de longitud a los 92 años. El aumento del número y tamaño de estas grietas se ha correlacionado positivamente con los resultados de tenacidad del hueso cortical (16).
Hueso Trabecular
Existen opiniones dispares en cuanto a establecer las propiedades biomecánicas del hueso trabecular. Hay autores que lo consideran con un modulo de elasticidad similar al del hueso cortical (15-20 GPa) (13). Otros autores, sin embargo le adjudican un valor de rigidez menor (0,75-10 GPa) (17). En cualquier caso se han determinado diferentes valores de E para el hueso trabecular en función de la prueba de esfuerzo utilizada y las condiciones del hueso esponjoso (seco, fresco o congelado), aunque siempre con valores menores que el hueso cortical. Los valores evidenciados son muy dispares incluso cuando los datos los emite un mismo autor aplicando el mismo ensayo a diferentes muestras (1,12).
McNamara y cols (18) desarrollaron un modelo sólido obteniendo 4 trabéculas de hueso vivo que posteriormente fueron procesadas con micro-CT y analizadas mediante elementos finitos. Este modelo permite observar la reacción a cargas sobre un modelo con morfología real (incluyendo lagunas de reabsorción activas). El estrés se observaba elevado en el fondo de las lagunas de reabsorción y aumentaría la actividad osteoclástica más allá de lo que inicialmente estaba previsto para renovar el hueso antiguo o dañado, y también evitan la distribución homogénea de la carga a lo largo de la trabécula.
Smit y Burger (19) establecieron la hipótesis que si la deformación baja (desuso) activa los osteoclastos, mientras que si la deformación aumenta (sobrecarga media) se activan los osteoblastos para rellenar la BMU. Estos datos se observaron con unas medidas de estrés no mayores de 16 Mpa y de deformación no mayores de 3.074 µε y con modelos informáticos de trabécula ideales (sin obtenerlas de trabéculas in vivo). Los datos de McNamara y cols (18) establecerían que aunque esto ocurriría habitualmente por debajo de 4.000 µε, existirían otros estímulos diferentes para activar a osteoclastos u osteoblastos cuando el estrés y las deformaciones son mayores de 4.000 µε.
Nivel Nanométrico (Molécula)
Durante muchos años se ha considerado que el hueso cortical y trabecular se consideraba un único material desde el punto de vista estructural molecular, y sus diferencias biomecánicas aparecerían en otras escalas debido a la diferencia de densidad. Está hipótesis ha sido rechazado por la evidencia en diferentes estudios de variaciones biomecánicas intrínsecas en los dos tipos de hueso. Si bien los componentes moleculares son idénticos, parece que la disposición de los mismos varía entre ambos influyendo en sus propiedades biomecánicas. Se han observado valores de módulo de elasticidad de 10,4 Gpa en el ensayo de tracción para la trabécula ósea, mientras que en las muestras de hueso cortical se encuentra en 18,6 Gpa (21).
Los dos componentes del hueso tienen propiedades mecánicas extremadamente diferentes. El mineral es duro y frágil, mientras que la proteína (húmeda) es mucho mas blanda pero más resistente (a la tracción, compresión, torsión, etc ). Sin embargo la unión de ambos (composite) combina las propiedades óptimas de cada uno, aportando dureza y resistencia (21). Un factor que va a condicionar las propiedades del hueso cortical o trabecular va a ser la proporción de placas minerales que contenga la matriz colagénica.
Vascularización del Seno Maxilar
La vascularización del seno maxilar es suministrada principalmente por la AAPS, la AIO y la AEP. La mucosa oral, los tejidos periósticos, la membrana sinusal y, especialmente, la pared anterolateral del seno están vascularizados por estas dos primeras arterias en un doble círculo arterial. Solar y cols.,26 describieron, a través de un esquema, el recorrido de los canales óseos que forman la anastomosis entre la AAPS y la AIO. Informaron que la anastomosis se extiende hasta la mitad de la pared lateral del seno maxilar, aproximadamente a una distancia entre 17 y 23 mm (de media 18,9 mm) del margen alveolar. Esto implica una menor probabilidad de sangrado durante el procedimiento de apertura de la ventana.
En cuanto a la anastomosis de las arterias sinusales, Traxler y cols.,14 encontraron una anastomosis intraósea entre la AAPS y la AIO en todos los especímenes examinados. En un estudio de Mardinger y cols.,32 tan solo el 50% de los casos, el vaso tenía el tamaño necesario para ser localizado por TC, al igual que en un estudio sobre cadáveres de Rosano y cols.,33 el canal óseo se localizó radiográficamente en un 47% de los casos, mientras Anamali y cols.,34 por medio de CBCT obtiene resultados >90%.
Se recomienda el uso de diagnóstico por imagen como parte imprescindible de la evaluación prequirúrgica y el plan de tratamiento para crestas severamente atróficas, con el fin de evitar el riesgo de sangrado severo. Se ha informado en la literatura actual que un riesgo de sangrado severo se puede dar cuando el diámetro del vaso es mayor a 2 mm36. Cuanto mayor es el calibre, mayor es el riesgo de una hemorragia profusa.
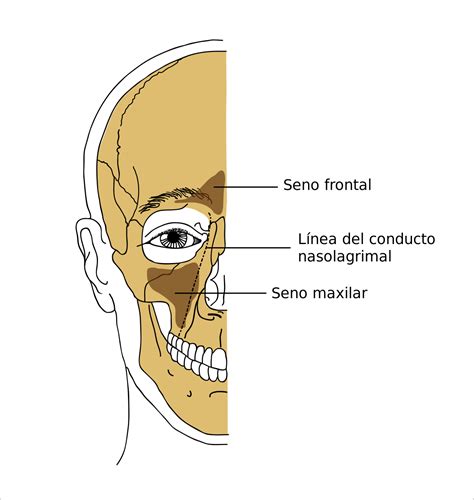
Vascularización del seno maxilar.
Consideraciones Quirúrgicas
Hay que considerar la vascularización durante el abordaje con ventana lateral debido a las posibles complicaciones durante el procedimiento quirúrgico28. En una serie de casos retrospectivos se informa sobre la ostectomía para el diseño de una ventana lateral, integrando tecnología piezoeléctrica junto con la instrumentación manual, siendo un medio actual eficaz para lograr la elevación de la membrana, al tiempo que minimiza el potencial de riesgos y complicaciones intraoperatorias.
Diversos autores obtienen que los diámetros máximos de la AAPS y la AIO pueden llegar a 2 y 2,7 mm, pero se da muy ocasionalmente22, 26, 28. Solar y cols.,26 informaron que el diámetro promedio de la AAPS en las imágenes por TC se encuentra en 1,6 mm y, de acuerdo con los estudios de Mardinger y cols.,32 afirman que los vasos con un diámetro <1 mm no representan un gran riesgo o una posible hemorragia durante los tratamientos quirúrgicos. Describieron que en la mayoría de los casos el calibre de la AAPS era inferior a 1 mm32. Solo el 29% de los casos tenían canales >1 mm y, por lo tanto, tenían riesgo de sangrado.
En el estudio de Ella y cols.,28 en 2008, llegaron a la conclusión de que en más del 10% de los casos existe riesgo de hemorragia debido a una arteria con un diámetro de más de 0,5 mm. Los resultados del estudio de Güncü y cols.,22 informaron que la arteria tenía un calibre promedio de 1,3 mm. De acuerdo con los resultados de los autores anteriores, en nuestro estudio también encontramos que el diámetro de la arteria se comprendía entre 1 y 2 mm en la mayoría de los casos (32,52%), tanto en mujeres como en hombres, donde el promedio se obtuvo en 1,2 mm de diámetro. Las arterias con un calibre menor a 1 mm alcanzaron un 11,38%, con un promedio de 0,7 mm de diámetro.
Las diferencias entre los resultados obtenidos en diversos estudios al medir el diámetro de la AAPS probablemente se deba a la resolución de los escáneres, a los diferentes criterios de inclusión y exclusión considerados y/o al menor número de muestras examinadas de los estudios27.
| Arteria | Diámetro Promedio (mm) | Riesgo de Hemorragia |
|---|---|---|
| AAPS | 1.6 | Bajo si < 1mm |
| AAPS | Varía entre 1 y 2 en la mayoría de los casos | Considerable si > 0.5mm |
| AIO | Hasta 2.7 (ocasional) | Potencialmente alto |
Diámetros promedio de las arterias maxilares y riesgo de hemorragia.
Músculos de la Mandíbula
Los músculos desempeñan un papel crucial en la función y biomecánica de la mandíbula.
- Masetero: Este músculo masticador cuadrangular se une desde el lado de la rama de la mandíbula a cada lado de la mandíbula al cráneo por encima. El masetero eleva y protruye la mandíbula, cerrando así la mandíbula.
- Temporal: Este extenso y potente músculo masticador en forma de abanico se origina en el hueso temporal del cráneo y se une a la rama de la mandíbula y a su apófisis coronoides. El músculo temporal eleva la mandíbula, cerrando los maxilares.
- Pterigoideo lateral: Este músculo tiene un aspecto cónico que se origina en la parte inferior del hueso temporal y los huesos esfenoides del cráneo y se une al cuello de la mandíbula, así como a la cápsula y el disco articular de la articulación temporomandibular. Actuando solos, los músculos pterigoideos laterales producen movimientos laterales de la mandíbula.
- Pterigoideo medial: Este músculo cuadrilátero comienza en el cráneo y se inserta en la superficie interna de la rama de la mandíbula. Los músculos pterigoideos mediales ayudan a elevar la mandíbula, cerrando los maxilares. Actuando juntos, ayudan a protruir la mandíbula.
🥇 MANDÍBULA - (MAXILAR INFERIOR), Anatomia. Fácil, Rápida y Sencilla
Si el tema de la anatomía llama tu atención estás de suerte. Estarás equipado con los conocimientos anatómicos necesarios para solicitar estudios posteriores en el campo de la medicina o la sanidad aliada.