La regeneración de encías es un campo en constante evolución dentro de la odontología, con el objetivo de encontrar soluciones efectivas para la enfermedad periodontal y la pérdida de dientes. Las investigaciones recientes se centran en el uso de células madre y nuevas técnicas de implantes que prometen revolucionar los tratamientos dentales.

Células Madre y su Impacto en la Regeneración de Encías
Cambiar la respuesta de las células madre a la inflamación puede tener efectos muy beneficiosos para la salud de las encías, pudiendo incluso revertir la presencia de enfermedad periodontal. Para el estudio, el equipo extrajo células madre de muelas del juicio y las colocó en placas de Petri, creando un entorno de enfermedad periodontal inflamatoria simulada en las placas de Petri.
A continuación, agregaron dos tipos específicos de moléculas sintéticas llamadas Maresin-1 y Resolvin-E1, ambos mediadores lipídicos especializados en pro-resolución de ácidos grasos omega-3. Tanto Maresin-1 como Resolvin-1 reprogramaron el fenotipo celular de las células madre humanas, demostrando que incluso en respuesta a la inflamación es posible aumentar la capacidad de las células madre para que puedan volverse regenerativas. Este hallazgo es importante porque permite a los científicos identificar las vías proteicas específicas involucradas en la inflamación.
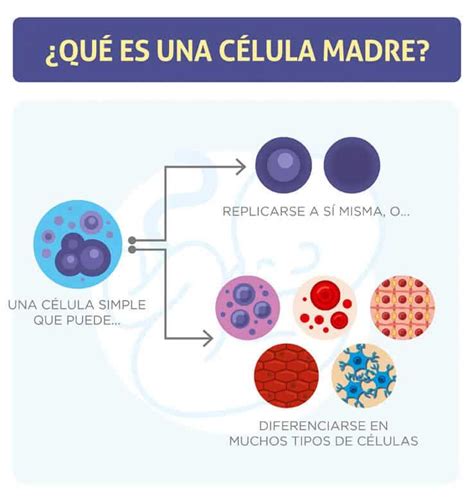
Estudio Experimental sobre Células Madre Humanas
Un estudio experimental evaluó el potencial y la estabilidad de la utilización de células madre mesenquimales (MSC) en la regeneración periodontal de la estructura original. Su objetivo es determinar un método de regeneración de la estructura periodontal original que se ha perdido después de la enfermedad periodontal, cerca de los elementos dentales vitales sin patologías correlacionadas.
Este estudio constituye una experimentación de fase 1 aprobada por el Instituto Superior de Salud sobre un número limitado de pacientes, cuyo objetivo principal será la evaluación de la biocompatibilidad y toxicidad in vivo de las células madre mesenquimales diferenciadas en sentido osteoblástico, sostenidas por andamios de colágeno biomiméticos en pacientes afectados por periodontopatía severa.
El protocolo describe el transplante de células madre mesenquimales derivadas de muestras de un aspirado percutáneo de médula ósea. Las células de la médula ósea son manipuladas ex vivo para el aislamiento de la población de células madre mesenquimales. Después de una fase de expansión celular, estas células se introducen en una estructura biomimética (andamios en colágeno), y se inducen a la diferenciación en sentido osteogénico.
El producto final que consta de andamios y células mesenquimales diferenciadas en sentido osteoblástico, se instala por último en el defecto alveolar periodontal. La experimentación se basa en la posibilidad de utilizar células madre mesenquimales autólogas a partir de la médula ósea humana. La finalidad es la de estimular la regeneración de PDL cerca de la pared radicular y la formación de hueso nuevo sobre el PDL, beneficiándose de las técnicas de regeneración-reconstrucción ósea, de manera que se recree la correcta anatomía periodontal.
Los resultados presentados en este trabajo conciernen el primer paciente tratado con esta metodología y afectarán los estudios siguientes para la prueba con una cobertura más amplia.
Células Madre Mesenquimales Orales: Estado del Arte en Odontología
Desde la organogénesis y hasta estadios adultos, las células madre mesenquimales participan activamente dando origen y manteniéndola homeostasis del organismo. En la cavidad oral han sido aisladas desde variadas estructuras del órgano dental tales como el ligamento periodontal, pulpa dental, tejido gingival, folículo dental y papila apical significando una prometedora fuente de células madre mesenquimales las que pueden ser caracterizadas de acuerdo a los criterios mínimos establecidos por "The International Society for Cellular Therapy".
Estos criterios son:
- La adherencia al plástico.
- La expresión de marcadores CD73, CD90, CD105 y la carencia de CD34, CD45, CD14, CD11, CD79, CD19 y HLA-DR (clase II).
- Capacidad multipotencial de diferenciación hacia linaje osteogénico, condrogénico y adipogénico.
El objetivo de esta revisión consiste en realizar un levantamiento de la situación actual de este tema efectuando una revisión comprensiva de la literatura en los campos de; identificación a través demarcadores de superficie, aislamiento por medio de mecanismos de digestión enzimática o explante, almacenamiento atendiendo a la necesidad de suprimir el uso de suero fetal bovino como medio de cultivo en un esfuerzo por avanzar hacia aplicaciones terapéuticas, banca o criopreservación destacando nuevas experiencia en este campo como lo es la criopreservación de piezas dentales completas gracias a la tecnología láser Nd:YAG. Y, finalmente, las aplicaciones clínicas que promete este grupo de células a través de la medicina regenerativa y la ingeniería tisular tanto en el campo de la odontología como la medicina general.

Nuevos Implantes que Crecen en la Encía
Un equipo de investigadores ha desarrollado un nuevo implante que crece en la encía y se fusiona con los nervios existentes para imitar la forma y la sensación de tener un diente real. La operación, aseguran, es mucho más sencilla que la del procedimiento que se usa actualmente y no es tan invasiva porque no requiere perforar el hueso. Millones de personas en el mundo han recurrido a los implantes para reemplazar los dientes perdidos.
Estas prótesis son visualmente muy similares a las piezas dentales reales y, por lo que se sabe por las pocas décadas que se llevan aplicando, también son muy duraderas. Sin embargo, cualquiera que haya sufrido una operación para colocarse implantes sabe que se trata de un procedimiento muy molesto y que las prótesis nunca acaban de sentirse como un diente de verdad.
Esto sucede porque los dientes son unas estructuras mucho más complejas de lo que parecen. “Los dientes naturales se conectan al hueso maxilar a través de tejido blando rico en nervios, que ayudan a percibir la presión y la textura y guían la forma en que masticamos y hablamos”, afirma Jake Jinkun Chen, profesor de periodoncia en la facultad de Odontología y Medicina de la Universidad de Tufts (EEUU). Chen es uno de los autores del estudio publicado en la revista Scientific Reports donde se presenta esta investigación.
“Los implantes carecen de esa retroalimentación sensorial”, asegura Chen. Esta limitación viene dada por su diseño: un pilar de titanio que se inserta directamente con el hueso maxilar y una corona, generalmente de cerámica, que se atornilla encima. Sin embargo, la perforación del hueso para colocar el pilar puede llegar a cortar o dañar nervios circundantes y provocar que dejen de ofrecer esta retroalimentación sensorial que notamos en los dientes naturales.
Cómo Funciona el Nuevo Implante
El implante desarrollado por el equipo de Tufts lleva un recubrimiento biodegradable que envuelve el implante de titanio. Este recubrimiento está impregnado de células madre y una proteína especializada diseñada para estimular su multiplicación y diferenciación en tejido nervioso, dicen los autores del estudio.
El recubrimiento se va disolviendo gradualmente durante el proceso de cicatrización, liberando sus componentes biológicos para favorecer el crecimiento de nuevo tejido nervioso alrededor del implante. Los investigadores quieren “reconectar los nervios”, permitiendo que el implante “se comunique con el cerebro de forma muy similar a un diente real”, asegura Chen.
La regeneración de los nervios no es el único beneficio del nuevo implante. Los investigadores aseguran que también incorpora partículas de goma similares a la espuma viscoelástica. Estas nanofibras se comprimen en un primer momento, permitiendo que el implante sea más pequeño que el diente perdido. Pero, una vez dentro, se expanden para garantizar un ajuste perfecto dentro de la cavidad dental.
Esta tecnología permite que la operación de inserción del implante sea mínimamente invasiva, dice el equipo. Los resultados de los estudios realizados con roedores son muy prometedores. Seis semanas después de la cirugía, los nuevos dientes permanecían firmemente anclados en las encías de los animales sin mostrar signos de inflamación o rechazo.
El análisis por imagen “reveló un espacio distintivo entre el implante y el hueso, lo que sugiere que el implante se había integrado a través del tejido blando en lugar de la fusión tradicional con el hueso”, señala Chen. Esta integración del tejido blando es clave para la posible restauración de la función nerviosa alrededor del implante y recuperar las sensaciones de un diente natural.
A pesar de este éxito con las pruebas iniciales, los investigadores apuntan a que esto es solo el comienzo y que hace falta profundizar más en su investigación. El equipo quiere realizar un estudio preclínico que confirme que los nervios recién formados alrededor del prototipo de implante transmiten con éxito la información sensorial. El siguiente paso, dicen, será realizar estudios en modelos animales más grandes para evaluar la seguridad y la eficacia del tratamiento.
Si se superan estas pruebas comenzarán los ensayos clínicos en humanos. "Este nuevo implante y esta técnica mínimamente invasiva deberían ayudar a reconectar los nervios, permitiendo que 'el implante se comunique' con el cerebro de forma muy similar a un diente real", explica Chen. "Este avance también podría transformar otros tipos de implantes óseos, como los que se utilizan en las prótesis de cadera o en la reparación de fracturas”.
La Regeneración Natural ya se Prueba en Humanos
La nueva medicina regenerativa está demostrando que en el futuro la pérdida de los dientes no tiene por qué ser definitiva. El objetivo de estas nuevas terapias regenerativas es aprovechar la propia biología humana para reparar o sustituir partes dañadas del cuerpo. En el caso de la odontología, estas innovadoras técnicas pueden regenerar los dientes perdidos sin tener que recurrir a materiales artificiales como implantes, empastes o prótesis dentales.
Uno de los fármacos más prometedores se ha desarrollado recientemente en el Hospital Universitario de Kioto y el Hospital Kitano de Osaka. El tratamiento es capaz de estimular el crecimiento natural de un tercer juego de dientes ocultos en nuestra boca. La terapia se lleva probando ya en humanos desde finales de 2024 y los resultados de estos ensayos clínicos deberían estar al caer.
Otra investigación, esta vez dirigida por un equipo de científicos del King' s College y el Imperial College, ambos en Londres, ha encontrado la manera de crear un diente cultivado en laboratorio a partir de células del propio paciente. El nuevo diente, dicen, puede integrarse fácilmente en la mandíbula y funcionar como un diente natural.
"Los empastes no son la mejor solución para reparar los dientes. Con el tiempo, debilitan la estructura dental, tienen una vida útil limitada y pueden provocar más caries o sensibilidad. Los implantes requieren una cirugía invasiva y una buena combinación de implantes y hueso alveolar. Ambas soluciones son artificiales y no restauran por completo la función natural del diente, lo que puede dar lugar a complicaciones a largo plazo", explica Xuechen Zhang, investigador de la facultad de Odontología y Ciencias Orales y Craneofaciales del King's College y uno de los autores de este descubrimiento.
Membranas para Regenerar Tejido Periodontal
Un equipo de investigadores de la UCLA (Estados Unidos) ha desarrollado una membrana que, probada en ratas, ayuda a regenerar tejido periodontal de las encías, lo que podría ayudar a tratar la periodontitis, una enfermedad crónica y destructiva que inflama las encías que rodean el diente, formando bolsas infectadas que conducen a la pérdida de huesos y dientes.
Los tratamientos actuales incluyen métodos para combatir infecciones como, por ejemplo, la aplicación de moléculas que promueven el crecimiento de tejidos, también conocidos como factores de crecimiento, o la regeneración tisular guiada, la cual se considera el estándar óptimo de atención para el tratamiento de la periodontitis. Para este último procedimiento se requiere el uso de una membrana o película delgada que se coloca quirúrgicamente entre la encía inflamada y el diente.
Estas membranas están destinadas a actuar no solo como barreras entre la infección y las encías, sino también como un sistema de suministro de fármacos, antibióticos y factores de crecimiento al tejido de las encías. Desafortunadamente los resultados de la regeneración tisular guiada son inconsistentes, dado que las membranas actuales carecen de la capacidad de regenerar directamente el tejido de las encías, no pueden mantener su estructura y estabilidad cuando se colocan en la boca y tampoco pueden soportar la administración prolongada de medicamentos.
Además, en las membranas no biodegradables se necesitan múltiples cirugías para eliminarlas después de que se hayan liberado los medicamentos, lo que compromete el proceso de curación. “Dadas las desventajas actuales de la regeneración tisular guiada, vimos la necesidad de desarrollar una nueva clase de membranas que tuvieran propiedades de regeneración tisular y ósea, junto con un recubrimiento flexible que pueda adherirse a una variedad de superficies biológicas”, han dicho los expertos.
Para ello, los investigadores comenzaron con una molécula sintética a gran escala comúnmente utilizada en aplicaciones biomédicas y que está aprobada por la Agencia Americana del Medicamento (FDA, por sus siglas en inglés). Debido a que la superficie de este polímero no es adecuada para la adhesión celular en el tratamiento periodontal, los investigadores introdujeron un recubrimiento de polidopamina, un polímero que tiene propiedades adhesivas, puede adherirse a superficies en condiciones húmedas y acelera la regeneración ósea al promover la mineralización de la hidroxiapatita, mineral que forma el esmalte y el hueso.
Después de identificar una combinación óptima para su nueva membrana, los investigadores utilizaron el ‘electrospinning’, un método que fusiona dos sustancias, para unir el polímero con el recubrimiento de polidopamina. Al mismo tiempo, para mejorar las características estructurales y superficiales de la nueva membrana, utilizaron plantillas de malla metálica, junto al ‘electrospinning’, con el fin de crear diferentes patrones, o micro patrones, similares a la superficie de una gasa.
“Al crear un micro patrón en la superficie de la membrana, podemos localizar la adhesión celular y manipular la estructura de la membrana. De hecho, hemos podido imitar la compleja estructura del tejido periodontal y, cuando la colocamos, observamos que complementaba la función biológica en cada lado”, han dicho los expertos.
Frena la Infección y Promueve la Regeneración Ósea y Tisular
Para probar la seguridad y la eficiencia de su nueva membrana, los investigadores inyectaron modelos de rata con células madre humanas derivadas de gingival y células madre de ligamento periodontal humano. Después de ocho semanas de evaluar la degradación de las membranas y la respuesta del tejido, observaron que la membrana polimérica recubierta de polidopamina tenía niveles más altos de ganancia ósea, en comparación con los modelos sin membrana o una membrana sin recubrimiento.
Asimismo, y con el fin de adaptarse a una amplia gama de aplicaciones médicas y dentales, los investigadores también hallaron una manera de ajustar la velocidad a la que la membranas se degradaban cuando se insertaban en sus modelos. Para ello, agregaron y restaron diferentes agentes oxidantes y utilizaron bases de polímeros más ligeros antes de pasar por el proceso de ‘electrospinning’.
La capacidad de aumentar o disminuir las tasas de degradación ayudó a los investigadores a controlar el tiempo de entrega de los medicamentos a las áreas deseadas. “Hemos visto que nuestras membranas son capaces de frenar la infección periodontal, promover la regeneración ósea y tisular y permanecer en el lugar el tiempo suficiente para prolongar el suministro de medicamentos”, han zanjado los científicos estadounidenses.
Conferencia "Células madre: terapia regenerativa en odontología"
tags: #regeneracion #encias #celulas #madre