En el ámbito de la microbiología, la correcta recolección, transporte y manejo de muestras son cruciales para obtener resultados precisos y confiables. Uno de los medios de transporte más empleados, especialmente para muestras fecales, es el medio de Cary Blair.
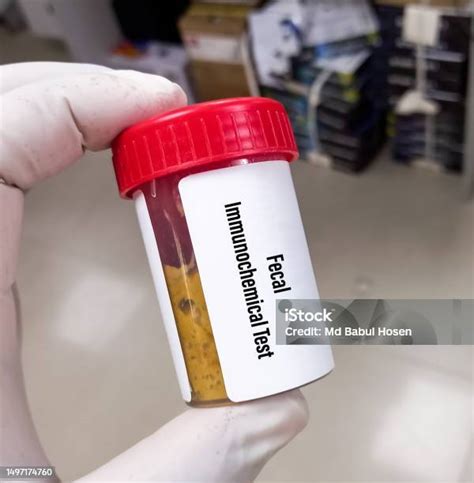
Recolección de muestra fecal para análisis microbiológico.
Importancia del Transporte Adecuado de Muestras
Los microorganismos presentes en una muestra pueden crecer, multiplicarse o morir rápidamente. Si alguno de estos eventos ocurre durante la recolección, el transporte o el almacenamiento, los resultados del laboratorio de microbiología podrían verse alterados. Por lo tanto, es esencial que las muestras se seleccionen, extraigan y transporten correctamente para optimizar su análisis e interpretación.
El transporte rápido de las muestras al laboratorio de microbiología es esencial para optimizar el rendimiento de los cultivos y la interpretación de los resultados. El retraso en el procesamiento de las muestras puede resultar en sobrecrecimiento de algunos microorganismos o la muerte de otros. También debe evitarse que la muestra se deshidrate.
Desde que la muestra es recogida hasta su procesamiento es fundamental que no se contamine, que no se produzca una proliferación excesiva de flora bacteriana y que los posibles microorganismos patógenos presentes en la muestra permanezcan viables. Para esto es importante que la muestra sea recogida, transportada y manipulada de forma adecuada.
Medios de Transporte: Garantizando la Viabilidad de los Microorganismos
Uno de los medios de recolección más empleados para muestras de tipo exudado son los hisopos. Se trata de varillas de madera o alambre con punta de algodón, alginato de calcio o dacrón. Existen en el mercado hisopos que van incorporados en tubos de plástico que contienen diversos medios de transporte. Una vez recogida la muestra, el hisopo se introduce en el medio de transporte.
Los medios de transporte consisten en agar semisólido, que carece de nutrientes pero que contiene agentes reductores cuya función es prolongar la viabilidad de los microorganismos. Un medio de transporte habitual es el conocido como medio de Stuart (agar semisólido amortiguado) que contiene tioglicolato de sodio como agente reductor. Este medio mantiene un pH favorable e impide tanto la deshidratación de las secreciones durante su transporte como al oxidación o autodestrucción enzimática de los patógenos presentes. Se utiliza para el transporte de exudados faríngeos, conjuntivales, nasales y heridas.
¿Qué es el Medio de Cary Blair?
El medio de Cary Blair es una modificación del medio de Stuart. Sus autores se dieron cuenta de que el glicerofosfato podía ser utilizado metabólicamente por algunas bacterias, generalmente saprófitas o acompañantes, que enmascaran a las patógenas al aumentar de número. Entonces lo sustituyeron por un tampón inorgánico fosfatado. Además, suprimieron el azul de metileno y aumentaron el pH a 8,4.
El medio de Cary y Blair se utiliza para el transporte de muestras fecales. El hisopo se coloca en medio de Cary Blair y se transporta a temperatura ambiente al laboratorio para cultivarlo en medio de TCBS. Es un medio destinado originalmente al transporte de microorganismos fecales, que también es utilizado con éxito para el transporte de anaerobios.
Medio de transporte Cary Blair para la conservación de microorganismos.
Tabla Comparativa de Medios de Transporte
A continuación, se presenta una tabla comparativa de diferentes medios de transporte:
| Medio de Transporte | Tipo de Muestra | Características |
|---|---|---|
| Medio de Stuart | Exudados faríngeos, conjuntivales, nasales y heridas | Agar semisólido amortiguado con tioglicolato de sodio. Mantiene el pH y previene la deshidratación. |
| Medio de Cary Blair | Muestras fecales | Modificación del medio de Stuart con tampón inorgánico fosfatado y pH elevado. |
Recomendaciones Generales para el Transporte de Muestras
- En general, las muestras se envían a Microbiología en contenedores anti derrames estériles dentro de bolsas de plástico selladas.
- En el caso de muestras de fluidos obtenidas en jeringa (líquido ascítico, drenajes, abscesos) la mayoría de los microorganismos permanecen viables en la jeringa durante periodos de tiempo significativos.
- Las muestras deberían llegar al laboratorio de 1 a 2 horas tras la extracción como máximo. Si el retraso es inevitable, las muestras deben ser conservadas de forma adecuada.
- Como norma general, las muestras deben ser refrigeradas a 4-6ºC. El período de refrigeración varía con el tipo de muestra.
- Las muestras normalmente asépticas, como la sangre o líquido cefalorraquídeo (LCR), no deben refrigerarse sino conservarse a temperatura ambiente, en el laboratorio de microbiología se conservan en estufa a 37ºC.
Es importante que el personal de laboratorio notifique al médico responsable lo antes posible el rechazo de la muestra para que puedan tomarse las medidas adecuadas para obtener nuevo material. En las situaciones en las que no puede obtenerse una nueva muestra (ej procedimiento invasivo o quirúrgico), el laboratorio puede analizar la muestra teniendo en cuenta que los resultados pueden estar comprometidos. En esos casos las decisiones se toman en colaboración entre el microbiólogo y el clínico y el informe de laboratorio generalmente se acompaña de un aviso.