En el ámbito ambulatorio, el profesional de la medicina se enfrenta a una serie de problemas al utilizar antibióticos para tratar las enfermedades infecciosas de la cavidad oral de forma racional. Estas dificultades surgen por las características propias de estos procesos y de las peculiaridades de la zona anatómica en que se establecen.
La mayoría de las infecciones de la cavidad bucal son inespecíficas, polimicrobianas (múltiples bacterias implicadas) y mixtas (bacterias con distinto tipo respiratorio). Por todo lo expuesto, a nivel ambulatorio se deben emplear casi obligatoriamente tratamientos antibióticos empíricos.
Antibioticos: CLINDAMICINA
Farmacología de los Antibióticos
Desde un punto de vista lingüístico se debería dar preferencia a la expresión «fármacos antiinfecciosos» para designar al grupo terapéutico conocido habitualmente por el término antibióticos. Un argumento más a favor es que el término antibiótico no ha sido utilizado nunca en sentido literal, sino que sirvió originalmente para distinguir a los fármacos antiinfecciosos de origen biológico (penicilina como producto del hongo Penicillium notatum) de aquellos obtenidos mediante síntesis química (sulfonamidas).
Los fármacos antiinfecciosos incluyen, además de las sustancias con actividad antimicrobiana, los antimicóticos, los virostáticos y los desinfectantes. En adelante se utilizará el término antibiótico como sinónimo de «sustancias con actividad antimicrobiana» y, por consiguiente, el artículo se centrará exclusivamente en este grupo de sustancias.
Los antibióticos ocupan una posición privilegiada entre la multitud de grupos de sustancias farmacológicas. Los representantes de otros grupos de principios activos farmacológicos influyen en alguna estructura o función del organismo humano, mientras que la acción de los antibióticos va dirigida a los microorganismos. Para el antibiótico ideal, el organismo humano constituye únicamente el espacio físico de acción.
Toda acción del antibiótico sobre una estructura del macroorganismo constituye un efecto adverso. Dado que los antibióticos aprobados se hallan más o menos alejados de la condición ideal de actuar exclusivamente sobre los microorganismos, la evaluación de un antibiótico se basa en la siguiente relación triangular: principio activo-macroorganismo-microorganismo (fig. 1).
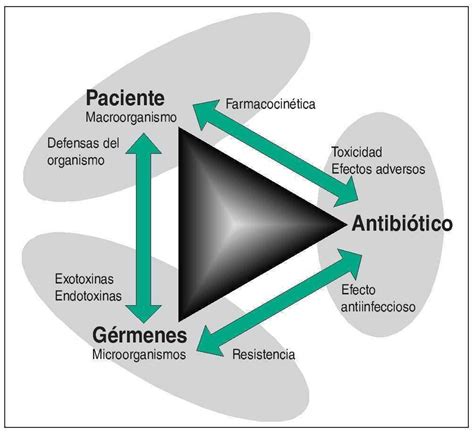
Figura 1. Relación triangular: antibiótico, macroorganismo y microorganismo.
En realidad, el uso de los antibióticos se enmarca en circunstancias más complejas. No basta con tener en cuenta la sensibilidad del o de los gérmenes implicados en la infección existente y los posibles efectos adversos en el sujeto tratado, sino que también se ha de valorar el beneficio del uso terapéutico (y más aún del uso preventivo) para el individuo en relación con el riesgo de acelerar el desarrollo de resistencias y, por ende, de perjudicar a la comunidad.
Por consiguiente se debe contraponer el beneficio del uso en el individuo frente al riesgo de la pérdida de sustancias y grupos de sustancias con una gran actividad antimicrobiana.
Lugares de Acción de los Antibióticos
La inhibición de los microorganismos se consigue fundamentalmente por las diferencias estructurales y funcionales de la célula bacteriana (fig. 2):
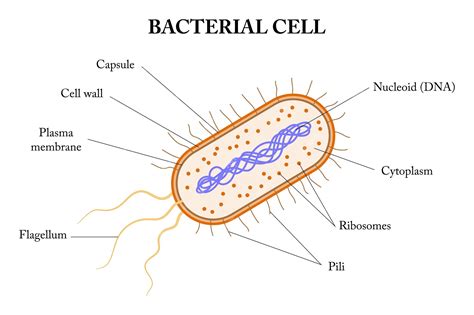
Figura 2. Representación esquemática de una célula bacteriana.
- El grupo de los antibióticos β-lactámicos (penicilinas, cefalosporinas) se aprovecha de la circunstancia de que la célula bacteriana no dispone sólo, como el resto de las células, de una membrana celular, sino que posee también una pared celular. Parece lógico que la alteración de la síntesis de la pared celular provocada por el antibiótico β-lactámico sólo dañe al microorganismo, sin influir en el macroorganismo, de lo que se deriva una relación beneficio-riesgo favorable.
- Los representantes del grupo de los aminoglucósidos, los macrólidos y las tetraciclinas interfieren en la biosíntesis proteica de las bacterias. Una serie de diferencias estructurales mínimas en los ribosomas favorece la selectividad del efecto sobre los microorganismos.
- Los inhibidores de la girasa (inhibidores de la topoisomerasa ~ fluoroquinolonas) y los nitroimidazoles inhiben la replicación del ADN. En el caso de los inhibidores de la girasa, la selectividad microbiana viene determinada por diferencias estructurales y funcionales de las topoisomerasas responsables de la formación de la doble hélice de cadenas de nucleótidos. En el caso de los nitroimidazoles (metronidazol), el depósito de un producto de reacción generado en el medio anaerobio provoca roturas de cadena, lo que explica su efecto selectivo sobre los gérmenes anaerobios.
- Las sulfonamidas compiten con el ácido p-amino-benzoico durante la síntesis del ácido tetrahidrofólico en las bacterias. La célula eucariota depende del aporte exógeno de ácido fólico, es decir, carece de la capacidad de sintetizar ácido fólico, por lo que no resulta dañada por la acción de las sulfonamidas.
- Por último, los polienos y los azoles son principios activos que modifican la permeabilidad de la membrana celular. Debido a la similitud de esta estructura celular en las células procariotas y las células eucariotas, no se consigue una gran selectividad. Por lo tanto, su tolerabilidad es relativamente menor en comparación con otros antibióticos.
Por motivos evidentes, se aspira a conseguir una gran selectividad, aunque esto no asegura forzosamente una buena tolerabilidad, dado que los principios activos pueden tener efectos totalmente independientes de su efecto antimicrobiano.
Además del perfil de efectos adversos que puede diferir entre los distintos grupos de sustancias e incluso entre los diferentes principios activos, todos los tratamientos antimicrobianos se asocian a un riesgo de alteración de la flora oral, colónica y vaginal. La alteración de la colonización fisiológica en estas cavidades orgánicas puede dar lugar a la proliferación de especies cuyo crecimiento es inhibido en condiciones normales por poblaciones competidoras de la flora fisiológica.
La colonización por gérmenes no fisiológicos explica la frecuencia de trastornos gastrointestinales, enteritis y cistitis crónicas recidivantes durante y después del tratamiento antibiótico.
Efecto Bacteriostático vs. Bactericida
Además de la clasificación en función de su mecanismo de acción, los antibióticos se pueden diferenciar por su acción bactericida o su acción bacteriostática. Esta diferencia es importante para el tratamiento. Los principios activos con acción bactericida dependiente de la concentración deben administrarse a dosis altas durante un período de tiempo corto, mientras que en el caso de las sustancias bacteriostáticas y las sustancias con acción bactericida dependiente del tiempo es más importante mantener concentraciones antibacterianas eficaces durante un período de tiempo más largo.
Se quiere advertir aquí de este hecho para evitar que las recomendaciones para una administración a corto plazo, incluso a dosis únicas, de un determinado antibiótico se trasladen sin más consideraciones a otros antibióticos. Una pauta de administración que puede estar justificada en el caso de los aminoglucósidos con acción bactericida dependiente de la concentración no es válida para los antibióticos β-lactámicos con acción bactericida dependiente del tiempo.
Los principios activos bacteriostáticos y los bactericidas muestran una cinética de inhibición diferente. Los dos principios activos, el bacteriostático y también el bactericida, inhiben el crecimiento bacteriano como muestra la figura 3. En el caso del principio activo bactericida, la población bacteriana disminuye de forma más rápida y más acusada. Sin embargo, ninguno de los principios activos consigue la erradicación completa de la población bacteriana.

Figura 3. Evolución cronológica de la eficacia antimicrobiana de principios activos bacteriostáticos y principios activos bactericidas.
El tratamiento antibiótico es capaz de reducir la población microbiana, pero para lograr la erradicación de los gérmenes residuales deben intervenir las defensas del organismo. La importancia de un sistema inmunitario intacto se pone de manifiesto con especial contundencia en vista de la gravedad que pueden adquirir las infecciones más triviales en pacientes inmunodeprimidos.
Parámetros del Efecto Inhibitorio y de la Resistencia
La concentración mínima inhibitoria (CMI) o la concentración mínima bactericida (CMB) son las concentraciones de una sustancia con actividad antimicrobiana que inhiben el crecimiento in vitro de una determinada cepa bacteriana o disminuyen la población de gérmenes vitales.
Los gérmenes se califican de resistentes si para su inhibición o destrucción hacen falta concentraciones más altas de un principio activo que las que se alcanzan en el organismo a dosis terapéuticas.
Lamentablemente, la CMI y la CMB no son valores inmutables de la potencia de un antibiótico que una vez establecidos sirven para siempre, dado que la sensibilidad de una especie bacteriana frente a un principio activo antibiótico puede ir disminuyendo. El desarrollo de resistencia se debe, bien a una selección de gérmenes menos sensibles, bien a mutaciones en las bacterias como consecuencia de las cuales se activan funciones o enzimas a través de las que la bacteria se puede sustraer a la acción antibiótica (resistencia secundaria).
Tratamiento Antibiótico en Odontología
El procedimiento ideal para elegir un antibiótico y determinar la dosis adecuada es la identificación del germen o de los gérmenes y la determinación de su sensibilidad frente a los antibióticos disponibles. Por motivos técnicos y de tiempo, este procedimiento se aplica sólo en casos excepcionales en la consulta dental.
En su lugar, la elección del antibiótico se orienta habitualmente por datos estadísticos de frecuencia con la que se identifican los gérmenes en una determinada infección y por la sensibilidad de éstos, estudiada recientemente en uno de los institutos microbiológicos regionales.
Antes de exponer situaciones terapéuticas concretas hay que resaltar que la administración de antibióticos no suele ser la medida más importante ni tampoco la única en el tratamiento de las infecciones odontogénicas. Este comentario previo es importante, dado que este artículo se centra en los principios activos antiinfecciosos. En el caso de los abscesos, por ejemplo, el drenaje quirúrgico es el tratamiento de elección y el tratamiento antibiótico sólo cumple una función complementaria.
Infecciones Odontogénicas
En general, las infecciones odontogénicas son infecciones mixtas, es decir, en ellas están implicados varios gérmenes patógenos. Hasta hace algunos años, se recomendaba administrar penicilina V como tratamiento de elección. La aparición de nuevos datos respecto a la situación de las resistencias, sobre todo de gérmenes anaerobios en infecciones odontogénicas, obligó a la comisión de expertos de la Sociedad Paul Ehrlich a revisar esta recomendación: la penicilina V es sustituida por una aminopenicilina combinada con un inhibidor de la β-lactamasa.
A diferencia de la penicilina V, el efecto inhibitorio de las aminopenicilinas incluye entre el espectro de gérmenes habitual algunas especies patógenas gramnegativas.
Aminopenicilinas
Las aminopenicilinas disponibles incluyen la ampicilina y la amoxicilina. La amoxicilina se absorbe casi totalmente (70-95%) después de la administración oral, mientras que en el caso de la ampicilina la absorción se reduce al 40%. La fracción no reabsorbida de la ampicilina, es decir, la que permanece en la luz intestinal, daña la flora intestinal. Por lo tanto, el tratamiento con ampicilina se asocia a menudo a trastornos gastrointestinales. Éste es el motivo por el que se recomienda cambiar a amoxicilina, al menos para el tratamiento oral.
Con las penicilinas se obtienen concentraciones tisulares (también óseas) suficientemente altas. La amoxicilina se elimina por vía renal. Su semivida de 1-2 h es aproximadamente dos veces mayor que la de la bencilpenicilina. Las aminopencilinas se descomponen y, por consiguiente, se inactivan por acción de la enzima β-lactamasa.
Dado que la resistencia frente a la penicilina se basa en gran parte en la inducción de la β-lactamasa bacteriana es útil combinarla con un inhibidor de la misma.
Clindamicina
Clindamicina penetra en los tejidos orales y también es activa frente a los anaerobios penicilin-resistentes. Como sabemos, la mayor parte de los gérmenes anaerobios que se hallan en las infecciones orofaciales son sensibles a las penicilinas, eritromicinas, clindamicina, doxiciclina y metronidazol.
Clindamicina, en combinación con otros fármacos antiprotozoarios, es efectiva en el tratamiento de las siguientes infecciones:
- Encefalitis toxoplásmica en pacientes con SIDA. La asociación de clindamicina con pirimetamina ha demostrado ser eficaz en aquellos pacientes que presentan intolerancia al tratamiento convencional.
- Pneumonía por Pneumocystis carinii en pacientes con SIDA. Clindamicina puede utilizarse en combinación con primaquina en aquellos pacientes que no toleran o no responden adecuadamente al tratamiento convencional.
- De forma tópica está indicado en el tratamiento del acné y de vulvovaginitis.
La dosis, vía de administración y duración del tratamiento deben determinarse en función de la gravedad y tipo de infección, del estado del paciente y de la susceptibilidad de los microorganismos causantes o sospechados. Puede emplearse vía oral, IV, IM o tópico.
- Vía oral: 8-30 mg/kg/día en 3-4 dosis. Máximo 1,8 g día.
- Vía intravenosa o intramuscular:
- Recién nacidos: 15 a 20 mg/kg/día, fraccionada en 3 o 4 dosis. En niños prematuros de poco peso pueden ser suficientes dosis más bajas (10-15 mg/kg/día).
- Lactantes y niños mayores: 20 a 40 mg/kg/día, fraccionada en 2, 3 o 4 dosis. Dosis máxima recomendada 2,7 g/día. En situaciones de riesgo vital se han administrado dosis de hasta 4,8 g/día por vía intravenosa.
La clindamicina no debe administrarse en bolo, para la administración intravenosa precisa de dilución previa. La infusión intravenosa debe ser realizada en al menos 10 a 60 minutos. La concentración de clindamicina en el diluyente no debe sobrepasar los 12 mg/ml y el porcentaje de infusión no debe exceder de 30 mg/minuto. No se recomienda administrar más de 1.200 mg en una sola infusión de 1 hora.
No se recomienda la administración de más de 600 mg en inyección única por vía intramuscular.
- Vía tópica:
- Vulvovaginitis: crema y óvulos vaginales, dosis habitual 1 aplicación al día durante 3 días. Limitada experiencia en menores de 16 años.
- Acné: Clindamicina: aplicar 1-2 veces al día en las áreas afectadas. Combinaciones con peróxido de benzoilo: aplicar una vez al día por la noche en las áreas afectadas. Lavar y secar la piel cuidadosamente previamente a la aplicación. El tratamiento no debe exceder las 12 semanas de uso continuado. Habitualmente no indicado en menores de 12 años.
Debe ser administrada con precaución a pacientes con antecedentes de enfermedad gastrointestinal, especialmente diarrea, colitis ulcerosa, enteritis regional o colitis asociada a antibióticos. En general no se requiere ajuste de dosis excepto en casos de deterioro grave de la función renal o hepática.
Se recomienda realizar estudios periódicos de la función hepática y renal, así como recuentos sanguíneos, especialmente en casos de terapia prolongada.
No debe ser utilizada en el tratamiento de infecciones del sistema nervioso central (por ejemplo, meningitis) dada su escasa penetración en el líquido cefalorraquídeo (LCR).
Algunas presentaciones comercializadas (consultar ficha técnica) contienen alcohol bencílico por lo que se deben extremar las precauciones en menores de 3 años por riesgos de toxicidad.
Efectos Adversos
Diarrea (el efecto adverso más frecuente entre un 10-20% de los pacientes), náuseas, vómitos, dolor gastrointestinal, flatulencia, incremento de enzimas hepáticas, mareo, dolor de cabeza, alteración del gusto y candidiasis vaginal.
El uso de clindamicina se ha asociado a colitis pseudomenbranosa por sobrecrecimiento de Clostridium difficile.
En el caso de tratamiento tópico para el acné: sequedad cutánea, eritema, sensación de quemazón, descamación, parestesia, irritación periocular, exacerbación del acné, prurito, reacciones gastrointestinales y dolor abdominal.
Interacciones
Posee propiedades bloqueantes neuromusculares y puede potenciar la acción de relajantes musculares no despolarizantes como los agentes curarizantes (pancuronio, tubocurarina, suxametonio) o los hidrocarburos anestésicos por inhalación (halotano, enflurano, isoflurano, dietiléter). En caso de administración simultánea se debe vigilar estrechamente a los pacientes debido a la posible prolongación del bloqueo neuromuscular.
Se ha demostrado antagonismo in vitro entre clindamicina y eritromicina, por lo que no se recomienda la administración simultanea de ambos.
Consideraciones especiales
Clindamicina atraviesa la barrera placentaria en humanos. Se han notificado casos en los cuales tras dosis múltiples, las concentraciones en el líquido amniótico eran aproximadamente el 30% de la concentración plasmática del fármaco en la madre. En estudios clínicos con mujeres embarazadas, la administración sistémica de clindamicina durante el segundo y el tercer trimestre no se ha asociado con un aumento de la frecuencia de anormalidades congénitas. No existen estudios suficientes y bien controlados con mujeres embarazadas durante el primer trimestre del embarazo.
Clindamicina se excreta en la leche materna tras la administración por vía oral o intravenosa, pudiéndose alcanzar concentraciones de 0,7 - 3,8 microgramos/ml.
Tabla resumen de dosis de clindamicina:
| Vía de Administración | Dosis | Frecuencia | Dosis Máxima |
|---|---|---|---|
| Oral | 8-30 mg/kg/día | 3-4 dosis | 1,8 g/día |
| Intravenosa/Intramuscular (Recién Nacidos) | 15-20 mg/kg/día | 3-4 dosis | - |
| Intravenosa/Intramuscular (Lactantes y Niños) | 20-40 mg/kg/día | 2-4 dosis | 2,7 g/día (hasta 4,8 g/día en casos graves) |
| Tópica (Vulvovaginitis) | Aplicación | 1 vez al día | 3 días |
| Tópica (Acné) | Aplicación | 1-2 veces al día | 12 semanas (uso continuado) |
tags: #clindamicina #en #odontologia #dosis