El término biofilm dental es desconocido para muchas personas. Sin embargo, conviene conocer bien de qué se trata y cómo se forma. Aunque no lo veas ni lo sientas en sus primeras fases, el biofilm representa una de las amenazas más importantes para dientes y encías.
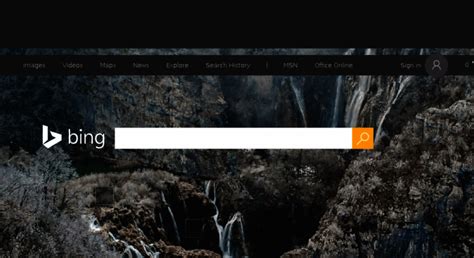
Ejemplo de biofilm dental
¿Qué es el Biofilm Dental?
El biofilm dental es mucho más que una simple placa bacteriana. A nivel práctico, muchos profesionales y pacientes utilizan ambos términos indistintamente. El biofilm no es solo una capa pegajosa sobre los dientes: es un sistema vivo capaz de alterar profundamente el equilibrio de la boca.
También conocido como pátina dental y, más comúnmente, como placa bacteriana, el biofilm dental tiene las mismas características que los biofilms microbianos que se forman en otros lugares del cuerpo, donde son capaces de propiciar la aparición de enfermedades específicas y muy graves.
En este punto, se debe tener en cuenta que la saliva juega un papel esencial a la hora de “barrer” las bacterias de la boca y neutralizar los ácidos. Por ello, si, a pesar de lavarte los dientes con frecuencia notas que acumulas mucha placa bacteriana y sarro, te aconsejamos acudir a una de nuestras clínicas dentales.
Las bacterias que se encuentran en la saliva pueden ser consideradas bacterias planctónicas (bacterias que flotan en una fase líquida). Sin embargo, las bacterias que se encuentran en una superficie dura (diente, reconstrucciones, prótesis e implantes) forman una película gelatinosa adherente: la placa dental.
La placa dental es el principal agente etiológico de la caries y de las enfermedades periodontales. El concepto y la apariencia de la placa dental han ido variando a lo largo de la historia dependiendo de los medios técnicos disponibles para su estudio.
Así, con la aparición del microscopio óptico, Anthony van Leeuwenhoek observó en 1683 que la placa dental estaba compuesta por depósitos blandos con microbios y restos de comida. Posteriormente, en 1898, Black definió la placa dental, como placas blandas gelatinosas.
Tipos de Biofilm Dental
- Supragingival: es aquel que se encuentra por encima de la línea de las encías.
- Subgingival: se sitúa por debajo de la línea de las encías.
El biofilm dental no siempre es claramente visible a simple vista; tiende a formarse principalmente en los espacios interdentales y cerca de la encía, es decir, en los espacios más difíciles de limpiar.
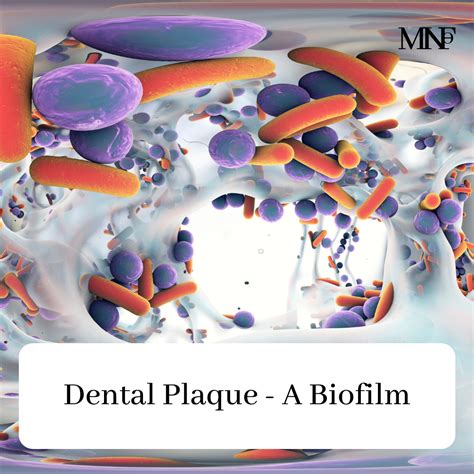
Tipos de biofilm dental
Formación del Biofilm Dental
La formación del biofilm dental es un proceso continuo y progresivo. Desgraciadamente, el proceso de formación del biofilm dental es muy rápido y, si no se interrumpe en una fase temprana manteniendo una higiene oral y profesional adecuada, pronto se convierte en el responsable de las enfermedades orales más comunes.
Antes de proceder a la explicación, conviene tener en cuenta que hay una gran cantidad de bacterias que viven en nuestra cavidad oral de manera natural. Nuestra boca es un entorno rico en microorganismos, incluidos los bacterianos, que tienden a organizarse en colonias para garantizar una mejor supervivencia.
El proceso de formación del biofilm dental sigue una pauta de colonización llamada sucesión autogénica, en la que los propios microorganismos inducen cambios físicos y químicos locales, que a su vez modifican la placa bacteriana. La colonización bacteriana se inicia con la formación de una película de proteínas salivares (albúmina, glucoproteínas, proteínas ricas en prolina ácida, mucinas, etc.) sobre el esmalte dental, a la que rápidamente se adhieren por especificidad bacilos y cocos gram positivos como S. sanguis, S. orallis, S. mitis y A.
Egelberg y cols determinaron los estadios en la formación de la placa dental:
- Un primer estadio o fase I, en la que se formaría una biopelícula sobre la superficie limpia del diente. Esta biopelícula estaría compuesta fundamentalmente por glicoproteínas.
- Un segundo estadio o fase II. En esta fase se observa la adhesión de unos determinados tipos de bacterias a la biopelícula previamente formada.
- Fase III. Se produce multiplicación bacteriana.
- Fase IV. Debido a la multiplicación bacteriana de la fase anterior y a la aparición de nuevas condiciones, se produce la coagregación de nuevas especies bacterianas.
En 1970, en el congreso de Edimburgo, se definió la placa dental como microorganismos más polisacáridos extracelulares; esta placa dental estaba recubierta por leucocitos, células epiteliales y restos de comida.
En los años 90, gracias al desarrollo y perfeccionamiento del microscopio confocal de láser, se llegó a un mejor conocimiento de la placa dental y de su estructura, y se desarrolló el modelo de la placa dental como biofilm.
A medida que la placa aumenta de grosor, la concentración de oxígeno en las zonas más profundas se reduce, por lo que las bacterias aerobias van desapareciendo de esta zona, siendo sustituidas por otras con un potencial de oxidorreducción más bajo. Biofilm oral multiespecie con aumento de anaerobios gram negativos ej. Fusobacterium, P.
Etapas de la formación del biofilm
- Adhesión: los microorganismos llegan a una superficie y se unen a ella gracias a la película adquirida o salivar.
- Colonización: Organización de los microorganismos de acuerdo con su especie en colonias.
- Crecimiento: aumento en número y especies de microorganismos del biofilm.
¿Cómo se desarrolla el biofilm?
Los biofilms pueden desarrollarse por medio de dos tipos de procesos:
- A partir de una célula planctónica
- A partir de otro biofilm
A partir de una célula planctónica
Ciertas bacterias muestran o tienen la capacidad de desarrollar estructuras de superficie que favorecen la adhesión de las mismas a una superficie sólida, tales como fimbrias y fibrillas. Así, colonizadores primarios como Actinomyces naeslundii, varias especies de estreptococos, como Streptococcus salivarius, Streptococcus parasanguis, Streptococcus mitis, muestran fimbrias y fibrillas en su superficie.
Otros factores que favorecen la adhesión de las bacterias a una superficie son la capacidad que muestran algunas especies bacterianas para el movimiento, como la Pseudomonas aeruginosa, Pseudomonas fluorescens, Escherichia coli, o la expresión de ciertas proteínas en su superficie celular, denominadas adhesinas.
Existen una serie de factores que afectan a la adhesión de las bacterias a una superficie sólida. Por un lado, factores físicos y químicos de la superficie, como su rugosidad y composición química, y factores del medio líquido en el que se desarrolla, como la velocidad del flujo y la composición química del mismo.
Una vez que las bacterias están ya adheridas a una superficie sólida se produce la expresión de ciertos genes que las diferencian de las formas planctónicas. Posteriormente se produce la multiplicación de la especie bacteriana y la coagregación con otras especies bacterianas. Dentro del biofilm, esta asociación de especies no sería aleatoria, sino que existirían asociaciones específicas entre bacterias dentro del biofilm.
A partir de otro biofilm
Los biofilms también se pueden desarrollar a partir de células sueltas desprendidas de un biofilm o de partes del propio biofilm. En cualquier caso, estas células desprendidas mantendrían todas las propiedades del biofilm de donde proceden. También se han descrito fenómenos de movimiento del biofilm sobre la superficie a la que se encuentra fijado.
Estructura del Biofilm
Cuando se observa un biofilm con el microscopio confocal de láser, pueden observarse las distintas comunidades bacterianas (dentro de las cuales pueden presentarse vacíos) organizadas en forma de seta o torre y separadas entre sí por microcanales de agua.
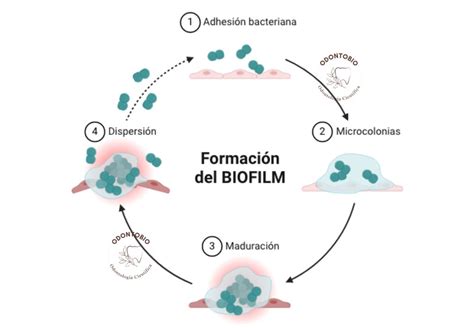
Estructura del biofilm
El biofilm está compuesto por bacterias, que representan un 15%- 20% del volumen, y una matriz o glicocálix, que representaría el 75% - 80%. Esta matriz está compuesta por una mezcla de exopolisacáridos, proteínas, sales minerales y material celular.
Los exopolisacáridos representan el componente fundamental de la matriz y son producidos por las propias bacterias del biofilm. Los exopolisacáridos participan de forma fundamental en el desarrollo del biofilm, pues su intervención mantiene la integridad del todo.
Pueden tener carga neutra o carga polianiónica, según el tipo de exopolisacárido, por lo que pueden interactuar con distintos antimicrobianos, de forma que estos últimos quedan atrapados en la matriz sin capacidad para actuar sobre las bacterias.
Los propios exopolisacáridos producidos por unas bacterias pueden actuar como fuente de nutrientes para otras bacterias y, de la misma forma, pueden atrapar otros nutrientes del medio y ofrecerlos a los distintos tipos bacterianos presentes en el biofilm, lo cual supone una ventaja para el desarrollo bacteriano.
Los exopolisacáridos actúan también retirando desechos del medio, lo que también favorece el desarrollo bacteriano. La composición química y la estructura terciaria de los exopolisacáridos determinan la capacidad de adhesión de los mismos lo que a su vez favorece la adhesión de las bacterias a las superficies.
Por último, los exopolisacáridos participan en funciones de protección de las bacterias, pues evitan su desecación. Además, gracias a sus cualidades pueden «tamponar» la acción de distintos antimicrobianos. La pérdida o alteración de un determinado polisacárido puede alterar el biofilm, o incluso puede producir la desaparición del mismo.
Propiedades de los Biofilms
Heterogeneidad fisiológica
Dentro del biofilm puede observarse un rango muy amplio de micronichos, separados unos de otros por mínimas distancias. Se pueden encontrar, asimismo, ambientes muy diferentes en cuanto al contenido de nutrientes del medio, tensión de O2, tensión de CO2, pH, etc.
Por lo tanto, células de la misma especie bacteriana pueden presentar estados fisiológicos muy diferentes, y también pueden encontrarse especies bacterianas con distintas necesidades fisiológicas (anaerobias, aerobias, microaerobias), separadas entre sí por sólo 10µm.
Fenotipos en el biofilm
Cuando las bacterias crecen en el biofilm, en forma sésil, manifiestan un fenotipo diferente respecto del que manifiestan cuando crecen en forma planctónica. Los fenotipos de las bacterias que crecen en los biofilms son más resistentes frente a diversos antimicrobianos y mantienen esta resistencia incluso cuando se desprenden del biofilm.
Señales en el biofilm
Dentro del biofilm, las bacterias tienen capacidad para comunicarse entre ellas, ya sea por medio de señales químicas o incluso mediante transferencia de material genético a través de mecanismos tales como la conjugación, la transformación, la transferencia de plásmidos y la transferencia de trasposones.
Dentro de dicha capacidad comunicativa mediante señales químicas es importante el fenómeno de «Quorum Sensing», es decir, la regulación de la expresión de ciertos genes a través de la acumulación de compuestos de señalización. Esta acumulación de señales químicas depende de la densidad bacteriana.
El «Quorum Sensing» puede proporcionar a los biofilms algunas de sus propiedades características, tanto en lo tocante al desarrollo de los mismos, como a la mayor resistencia frente a los antimicrobianos. Por ejemplo, puede promover la expresión de genes codificantes para la resistencia a un determinado antibiótico a partir de cierta densidad celular; tendría también capacidad para influir en la estructura del biofilm, estimulando el crecimiento de especies beneficiosas para el mismo e inhibiendo el crecimiento de las especies competidoras.
La capacidad que poseen las bacterias de comunicarse entre sí tiene influencia en la resistencia bacteriana frente a los antimicrobianos, en la producción de factores de virulencia y en la estructura del propio biofilm.
Capacidad adaptativa
Los biofilm deben mantener un equilibrio, por un lado, entre el crecimiento en condiciones favorables en cuanto a aporte de nutrientes y de medio ambiente, y por otro, el mantenimiento de su estructura. En condiciones desfavorables, el biofilm puede involucionar a estadios anteriores, pero en casi todas las situaciones se mantiene como parte del mismo y unido a la superficie, pudiendo volver a desarrollarse cuando las condiciones mejoran.
Ventajas de los biofilms
Una vez revisadas las propiedades del biofilm se constata que las bacterias que crecen en esta forma van a presentar una serie de ventajas:
- Protección frente a agresiones externas y mayor resistencia frente a los antimicrobianos.
- Ventajas nutricionales: aporte de nutrientes y eliminación de desechos.
- Proporciona un medio ambiente adecuado para el desarrollo bacteriano.
- Capacidad de intercomunicación entre las bacterias.
Resistencia frente antimicrobianos
Dentro de estas ventajas, merece la pena destacar la mayor resistencia frente a los distintos antimicrobianos. Esta cualidad puede deberse a:
- Los antimicrobianos van a llegar en menores concentraciones (concentraciones no efectivas frente a las bacterias) a las zonas profundas del biofilm.
- Las bacterias, al ser atacadas con dosis subletales tienen capacidad para desarrollar resistencia frente a los antimicrobianos (entrenamiento de resistencia con dosis subletales).
- Al crecer en forma sésil, las bacterias activan genes que proporcionan mayor resistencia frente a los antimicrobianos en comparación con las formas planctónicas.
- En zonas profundas del biofilm, que tienen un menor aporte de nutrientes, las bacterias estarían en forma quiescente, que es un estado bacteriano no susceptible a los antimicrobianos.
- Las bacterias estarían protegidas por la matriz de exopolisacáridos frente a los antimicrobianos.
Esta mayor resistencia de las bacterias cuando crecen en biofilm se traduce en que, para que sea efectivo, se deben multiplicar incluso por mil las concentraciones necesarias del antimicrobiano. Esto explicaría en parte por qué a veces no concuerdan los resultados clínicos con los resultados obtenidos in vitro.
Se ha visto que al crecer en forma sésil, las bacterias presentan mayor resistencia frente a los distintos antimicrobianos, por lo que se puede cuestionar que los distintos productos de los que disponemos sean realmente útiles. De hecho, se están desarrollando nuevas investigaciones en modelos de boca artificial dirigidos a comprobar la eficacia de los antimicrobianos frente a los biofilms.
De entre los distintos colutorios que existen en el mercado, solamente se han publicado estudios sobre colutorios de clorhexidina y colutorios de aceites esenciales, quedando demostrada en ambos casos la capacidad de los mismos para penetrar en el biofilm y producir una acción bactericida suficiente.
Enfermedades Causadas por los Biofilms
El biofilm dental desempeña un papel fundamental como precursor de las dos principales enfermedades bucales. La formación de estas biopelículas es posible en muchas zonas del cuerpo y, cuando se produce, es capaz de favorecer el nacimiento y el crecimiento de diferentes microorganismos, en especial de colonias bacterianas que pueden provocar una infección. Incluso teniendo un buen estado de salud, es normal encontrar diversidad de microorganismos en la boca.
Las bacterias del biofilm metabolizan los azúcares de los alimentos y generan ácidos que desmineralizan el esmalte. La acumulación de biofilm en el margen de las encías provoca inflamación, enrojecimiento y sangrado.
Algunas de las enfermedades causadas por el biofilm son:
- Caries
- Gingivitis
- Periodontitis: es la evolución de una gingivitis no tratada, que se puede resolver y mantener bajo control constante.
Enfermedades causadas por el biofilm dental
Cómo Controlar el Biofilm Dental
Aunque el biofilm no puede eliminarse del todo, sí puede mantenerse bajo control. Ya hemos mencionado que los azúcares son metabolizados por las bacterias en la boca y acaban generando una serie de ácidos que atacan el esmalte dental.
Cada vez que ingerimos alimentos y bebidas, hay bacterias que se acumulan en los dientes. Esto se debe a que, cuando comemos, las bacterias metabolizan los azúcares y carbohidratos de los alimentos, lo que produce unas sustancias ácidas que debilitan el esmalte dental.
En un primer momento, el biofilm dental es una película fina y blanda que se puede retirar fácilmente con un buen cepillado. En caso de no eliminar el sarro, las consecuencias que este provocará sobre la cavidad oral serán cada vez más dañinas.
Las sustancias y macromoléculas hidrofóbicas son atraídas y se adhieren a los dientes o las dentaduras. Si, mientras se trate de estadios tempranos donde una correcta higiene oral permita su eliminación. Una vez mineralizada y convertida en sarro dental, hay que evitar los métodos de autogestión. En estadios tempranos de su formación la placa dental en sí no es visible.
Algunos consejos para controlar el biofilm dental:
- Cepilla tus dientes al menos dos veces al día durante 2 minutos con una técnica adecuada, especialmente en la unión entre diente y encía.
- Hay que cepillar los dientes después de cada comida y usar una pasta dental con flúor. Por otro lado, es preferible utilizar un cepillo de dientes con cerdas suaves para evitar dañar las encías y el esmalte. Por eso, resulta recomendable usarlo después de comer o, al menos, una vez al día.
- El biofilm se acumula especialmente en zonas de difícil acceso.
- Algunos colutorios con agentes antiplaca, como la clorhexidina (de uso puntual) o el CPC, pueden ayudar a reducir la carga bacteriana en boca.
- Una limpieza dental profesional elimina el biofilm endurecido (sarro) y permite mantener a raya su progresión.
- Evita un exceso de azúcares, harinas refinadas y bebidas ácidas, ya que alimentan las bacterias del biofilm.
- Beber agua con regularidad es otra de las cosas que se pueden hacer para mantener el biofilm dental bajo control.
- Otro de los principales consejos para controlar el biofilm oral es acudir al dentista entre una y dos veces al año. De esta manera, el profesional podrá hacer una revisión y pautar la frecuencia idónea de las limpiezas bucodentales profesionales.
Aunque la higiene diaria es imprescindible, solo un dentista puede evaluar de forma precisa el estado del biofilm en tu boca.
¡COMO QUITAR EL SARRO 💩 DE LOS DIENTES EN CASA 🏡! ¡ES EN SERIO!
Únete a una comunidad dedicada a mejorar tu bienestar bucodental. Porque una boca sana es el inicio de un cuerpo saludable.