El pegamento dental es un producto que se emplea para fijar una prótesis a la boca del paciente. Si nos referimos al pegamento que usan los pacientes para conseguir la sujeción de la prótesis a la encía, hablamos de fijadores. Estos productos solo se aplican en prótesis de quita y pon, puesto que aquellas que son fijas no requieren de ninguna sustancia que las sujete a la boca. Conocer los efectos secundarios y el uso adecuado de estos productos es fundamental para mantener una buena salud oral.
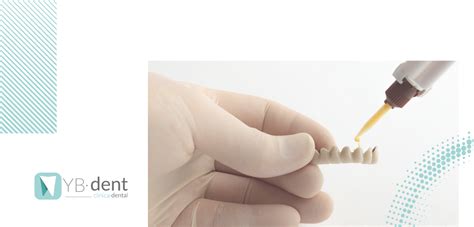
¿Cuándo y Cómo Usar el Pegamento Dental Correctamente?
Desde que comienzas a llevar la prótesis removible hasta que te adaptas a ella por completo pasará un tiempo. Es conveniente que los pacientes con prótesis removibles no las lleven puestas durante las horas de sueño, para que la mucosa descanse. Antes de aplicar cualquier tipo de adhesivo o fijador, es importante limpiar bien la prótesis. Tras secarla adecuadamente y con cuidado, aplicamos el pegamento dental en la prótesis. Evita echar demasiado producto para que no sobresalga.
Después, hacemos una ligera presión hasta notar que el aparato está bien sujeto. Lo normal es que solo sea necesaria una aplicación del adhesivo al día, así que el pegamento puede durar 12 horas. No obstante, un mal ajuste del aparato puede hacer que se mueva a pesar de haber aplicado un fijador.
Ahora que ya sabes qué tipo de pegamento dental debes usar para fijar tu prótesis removible, tan solo tienes que elegir entre las variadas marcas que ofrece el mercado. Las cremas fijadoras Corega son muy efectivas y duraderas, ya que permiten al paciente comer con normalidad sin sentir que la prótesis se mueve. Por último, la gama Algasiv ofrece almohadillas adhesivas para dentaduras postizas. Al cubrir la superficie de la prótesis que está en contacto con las encías, impide que se filtren alimentos y bebidas. Sea cual sea la marca por la que te decantes, así como si prefieres usar cremas frente a almohadillas, por ejemplo, lo importante es que apliques el producto correctamente.
Por ello, toda práctica alejada de este uso supone un uso indebido del pegamento dental.
Kukident: Cómo aplicar adhesivo en su dentadura
Riesgos y Efectos Secundarios del Uso Indebido
Usar demasiado adhesivo dental podría ser peligroso para la salud, sugirió un nuevo estudio. El equilibrio entre el zinc y el cobre en el organismo es fundamental para la salud neurológica. Ingerir demasiada cantidad de uno de esos metales puede causar deficiencia del otro.
Dos de las cremas fijadoras para prótesis dentales más populares, Corega Total y Corega Súper, dejarán de fabricarse al detectarse efectos secundarios en consumidores que han hecho un mal uso. Estas dos presentaciones contienen zinc y su ingesta en cantidades excesivas a lo largo de un periodo prolongado de tiempo se asocia con riesgos potenciales para la salud. La presencia de altos niveles de zinc en el organismo está asociada a una sensación de adormecimiento, hormigueo o debilidad en brazos y piernas, dificultades para caminar, trastornos del equilibrio y anemia.
En la revista Neurology, el equipo de la doctora Sharon P. Nations, del Centro Médico de la University of Texas, en Dallas, describió el caso de cuatro pacientes con dentaduras postizas que desarrollaron problemas neurológicos. Todos tenían niveles de zinc en sangre anormalmente altos y de cobre anormalmente bajos.
Los niveles normales de cobre oscilan entre 0,75 y 1,45 microgramos por mililitro (mL), pero en los participantes eran de menos de 0,1 a 0,23 microgramos por mL. El valor máximo normal para el zinc en sangre es de 1,10 microgramos por mL, pero en los pacientes era de entre 1,36 y 4,28 microgramos por mL.
Los síntomas de un paciente eran debilidad y pérdida del equilibrio, mientras que otra paciente sentía una debilidad en los brazos y piernas que la obligaba a utilizar silla de ruedas, junto con deterioro cognitivo e incontinencia urinaria. Esos pacientes mostraron "una mejoría neurológica leve" tras suspender el uso de adhesivo y comenzar a consumir suplementos con cobre. Otro paciente consumió suplementos con cobre, pero no suspendió el adhesivo dental. Sus niveles de cobre mejoraron, pero los de zinc se mantuvieron demasiado altos y no desaparecieron los síntomas neurológicos. El cuarto paciente, que usó suplementos con cobre y suspendió el uso del adhesivo dental, logró equilibrar los niveles de cobre y zinc, sin reducir los síntomas neurológicos. Los análisis revelaron que las concentraciones de zinc que usaban los pacientes eran de entre 17.000 y 34.000 microgramos por gramo de adhesivo dental.
Reacciones Adversas y Biomateriales en Prostodoncia
La incidencia de reacciones adversas a los productos dentales es difícil de estimar. Los odontólogos usan productos potencialmente alérgicos e irritantes durante sus procedimientos dentales. Estos materiales incluyen antisépticos, anestésicos locales, radiación ultravioleta, guantes de látex, dique de goma, enjuagues y otros productos empleados en la higiene bucal. Adicionalmente, los materiales empleados durante los procedimientos restauradores como metales, materiales de impresión, cementos, acrílicos y adhesivos también pueden producir efectos indeseables en los tejidos de los pacientes.
La presentación de complicaciones orales producidas por estos materiales pueden incluir estomatitis, reacciones liquenoides, quemaduras bucales, queilitis, inflamación labial y facial, sintomatología general y anafilaxis.
Se ha informado en la literatura una gran cantidad de casos relacionados con reacciones tisulares orales a biomateriales empleados durante los procedimientos restauradores, sugiriéndose que algunos metales como el níquel o el cobre liberados de ciertas aleaciones podrían ser tóxicos debido a reacciones tisulares expresadas como inflamación gingival. Algunos estudios han informado liberación de metales a partir de aleaciones nobles y altamente nobles que han ocasionado decoloración e hiperplasia de la encía adyacente. Un considerable número de publicaciones han mostrado casos de alergias a materiales restauradores presentándose diferentes tipos de sintomatología intraoral.
Biocompatibilidad: Se define en el glosario de términos prostodóncicos como la capacidad de existir en armonía con el ambiente biológico circundante. En general, se calcula basándose en la citotoxicidad localizada, la respuesta sistémica, la alergenicidad y la carcinogenicidad y debe cumplir con los siguientes criterios: no ser dañino para la pulpa y los tejidos blandos, no contener sustancias tóxicas que se puedan difundir, liberar y absorber en el sistema circulatorio para causar respuesta tóxica sistémica, debe estar libre de agentes sensibilizantes que puedan llegar a causar respuestas alérgicas y no tener potencial carcinogénico.
Biomaterial: El cual se define como cualquier sustancia que se pueda usar por cualquier período de tiempo como parte de un sistema que trate, aumente o reemplace algún órgano, tejido o función del cuerpo. Con respecto a los materiales dentales se sabe que se usan en humanos por períodos de tiempo largo o corto. Se consideran que éstos son similares a otros materiales especializados usados en ortopedia, cirugía cardiovascular, cirugía plástica y oftalmología y que además están en contacto estrecho con diversos tejidos humanos.
Pruebas de Biocompatibilidad
- Grupo I o de pruebas primarias: Consisten en evaluaciones de citotoxicidad y genotoxicidad, en las que los materiales se ponen en contacto con cultivos celulares para determinar el efecto en la viabilidad celular e en el material genético.
- Grupo II o de pruebas secundarias: Evalúan la toxicidad sistémica, la dosis letal 50 (DL50), el grado de irritación y sensibilización que incluyen las pruebas de inhalación (para determinar toxicidad) y de implantación.
- Grupo III o pruebas de uso preclínico: Un producto puede ser aprobado por la Administración de Drogas y alimentos de los Estados Unidos (FDA) si supera las pruebas primarias y secundarias (realizadas en cultivos celulares y animales de experimentación); sin embargo, permanece en estudio y observación durante siete años más. Las pruebas terciarias se hacen para medir el efecto de los materiales que estarán en contacto con dentina y pulpa.
Basado en lo anterior se deduce que los materiales dentales antes de salir al mercado están sujetos a una serie de pruebas que garantizan que no son lesivos ni peligrosos para el ser humano: sin embargo, pueden llegar a producir efectos adversos que sólo pueden observarse con el tiempo y cuando se ponen en contacto con los tejidos.
Los efectos de cualquier material que entre en contacto con el cuerpo humano van desde ninguno hasta los que se describen más adelante, y dependen del grado de disolución en el cuerpo y la liposolubilidad, la vía de exposición (venosa, respiratoria, dérmica, oral) o de la vía de eliminación (la cual depende de la vía de administración). La mayoría de materiales odontológicos se localizan en la vía de exposición oral, la cual se considera como la menos peligrosa debido a que la absorción es la más lenta. Otros materiales como los implantes si se pueden considerar de alto riesgo porque su vía de exposición es la sanguínea, siendo la más peligrosa, debido a su rápida absorción.
Efectos Adversos de los Materiales Dentales
Los efectos adversos que pueden llegar a causar cualquier material sobre los tejidos incluyen:
- Citotoxicidad
- Teratogenicidad
- Carcinogenicidad
- Biodegradación
- Liberación de componentes
- Exposición y toxicidad
- Alergia e hipersensibilidad
- Alergia por contacto
Citotoxicidad: Es un mecanismo de toxicidad mediado inmunológicamente que produce muerte celular local ya sea por apoptosis o necrosis.
Genotoxicidad o teratogenicidad: Es un mecanismo de producción de malformaciones en el feto. Una sustancia teratogénica o genotóxica es aquella capaz de producir malformaciones durante el embarazo y el desarrollo futuro del niño.
Con respecto a los materiales dentales, se sabe que estos se liberan de manera gradual y lenta siendo muy poco probable que alcance las concentraciones pico que excedan el umbral para que lleguen a causar efectos teratógenos. Además hay diferencias bastante grandes entre la magnitud de exposición de un medicamento y un material dental, debido a que los segundos se consideran inertes y estables y la vía de exposición es oral, por lo tanto para que el material llegue a producir efectos teratogénicos debería ser administrado en altas dosis, ser altamente liposoluble y tener la capacidad de atravesar la barrera placentaria, lo cual es casi imposible con un material dental. En términos generales faltan hallazgos consistentes que demuestren verdaderas relaciones causales entre los materiales dentales y los defectos congénitos.
Carcinogenicidad: Consiste en la degeneración neoplásica en los animales o el hombre. Los estudios que se han hecho para evaluar la carcinogenicidad de los materiales dentales se han centrado en los implantes. Los dos mecanismos por los que se puede llegar a producir carcinogenicidad son el físico y el químico. El primero, está relacionado con el tamaño y la forma del implante, aplica a los cerámicos, polímeros y metales. En el hombre se ha relacionado de manera poco frecuente los mecanismos físicos con las neoplasias. Con respecto al mecanismo químico, se considera que es un proceso por medio del cual la célula pasa a través de múltiples estados hasta llegar a un clon de células que irreversiblemente se convierten en un tumor. Dentro de las especies involucradas en este proceso están los radicales libres y los productos inflamatorios. De los materiales dentales se sabe que son carcinogénicos el formaldehído, el cloroformo, fluoruros inorgánicos y algunos metales como el níquel, el cromo y el berilio.
Biodegradación: Se refiere a los procesos de destrucción y disolución de los materiales por la saliva o por acción física o química como el desgaste y la erosión, la masticación, los alimentos o la actividad bacteriana. Está altamente relacionado con la corrosión.
Corrosión: Se define como el proceso químico o electroquímico a través del cual un metal es atacado por agentes naturales tales como el agua o el aire, llevando a una disolución parcial deterioro o debilitamiento de una sustancia sólida. La corrosión puede ser crevicular, galvánica, de shock o de fisuras. Los efectos de la corrosión están relacionados con el daño del material y la toxicidad causada por la liberación y difusión de sustancias en el organismo.
En la boca hay gran posibilidad de que se produzca corrosión cuando se ponen restauraciones metálicas debido a la presencia de humedad, electroconductividad de la saliva, pH y presencia de alimentos. La corrosión se puede prevenir cubriendo el metal con materiales impermeables o con zinc, utilizando metales nobles, mediante electroplateado, usando metales resistentes a la corrosión como el cromo o realizando un pulido y terminado adecuado.
Liberación de los componentes: A partir de los materiales dentales es gradual y lenta. Se sabe que como resultado de la corrosión de los metales usados para las restauraciones, especialmente los metales base, se liberan metales como níquel, berilio, cromo, paladio y mercurio. También se liberan monómeros de metilmetacrilato a partir de los acrílicos usados para los provisionales y las bases protésicas.
Exposición y toxicidad: Son dos efectos que se producen en los tejidos por contacto con materiales liberados y pueden ocurrir de manera independiente o asociadas. La primera es el contacto con un xenobiótico y la toxicidad es el efecto adverso que resulta por el contacto con un xenobiótico.
Alergia e hipersensibilidad: Se define como una reacción inmunológica fuerte a sustancias que normalmente no representan peligro para el ser humano. Fundamentalmente hay cuatro tipos de reacciones alérgicas producidas por el contacto con materiales dentales: reacciones anafilácticas, mediadas por la inmunoglobulina E; reacciones citotóxicas, mediadas por la inmunoglobulina M o G; reacciones mediadas por complejos inmunes y activación del complemento, y las reacciones de hipersensibilidad retardada mediada por linfocitos T.
Alergia de contacto: Está basada en compuestos de bajo peso molecular que se vuelven inmunogénicos al entrar en contacto con proteínas del huésped. De esta manera se elaboran los antígenos que inducen sensibilización de células inmunocompetentes. Las características que presenta la alergia de contacto incluyen el hecho de ser adquirida, además es específica, consigue generar memoria y puede ser transformada por células. Un prerrequisito para que ocurra la alergia de contacto es que haya una unión estable entre el metal o la sal y la parte proteica rica en electrones. El níquel, el cromo y el cobalto han mostrado estas propiedades.
Biomateriales Usados en Prostodoncia y Sus Reacciones Adversas
Los materiales usados en prostodoncia se dividen en materiales de impresión, de restauración y cementos. Los efectos adversos que producen se presentan a continuación.
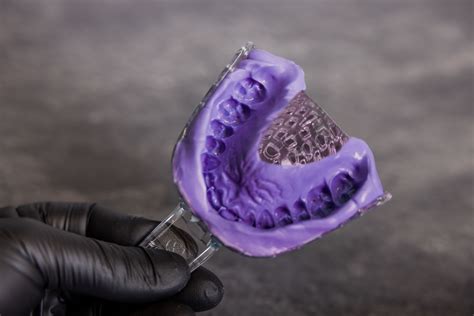
Materiales de Impresión
Los materiales de impresión pueden ser elásticos y no elásticos. Los no elásticos incluyen las ceras, el yeso y los materiales termoplásticos. Los materiales elásticos se clasifican en elastoméricos y los hidrocoloides. Los hidrocoloides abarcan los reversibles (tipo agar) e irreversibles (alginatos). Los elastoméricos incluyen las siliconas de adición y de condensación, los poliéter y los polisúlfuros.
No se conocen publicaciones que presenten los efectos adversos que pueden producir estos materiales, a excepción de reacciones alérgicas. Sin embargo, cuando se emplea un hilo retractor impregnado de sustancias con el fin de mejorar la separación del tejido gingival, la presencia de efectos adversos puede estar presente. Usualmente los hilos se impregnan de materiales vasoconstrictores, astringentes y sustancias hemostáticas. El cloruro de aluminio es un astringente y a la vez es un hemostático y como efecto adverso produce quemadura de los tejidos debido a que es una sustancia cáustica. Por lo anterior, su uso se debe limitar a casos en donde es muy difícil visualizar la línea de terminación.
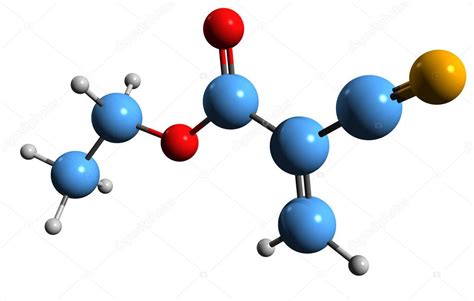
Cianoacrilato: Definición, Propiedades y Aplicaciones
El cianoacrilato es generalmente una resina acrílica, que polimeriza rápidamente en presencia de agua formando cadenas largas y fuertes. Son líquidos incoloros y de baja viscosidad. El metil-2-cianoacrilato se usa como componente del pegamento de cianoacrilato y su calentamiento provoca la despolimerización, produciendo elementos gaseosos muy irritantes para los pulmones y los ojos. El n-butil-cianoacrilato es un éter, insoluble en agua, incoloro y líquido. Su empleo principal es como componente de cianoacrilatos de uso médico.
La fuerza adhesiva de este compuesto depende de la polimerización de monómeros de cianoacrilato formándose uniones muy fuertes. Los ácidos débiles inhiben débilmente la polimerización, sin embargo los ácidos fuertes la paran completamente. La ruptura de este polímero puede hacerse con acetona (quitaesmalte de uñas, por ejemplo).
El cianoacrilato puede ser sintetizado por reacción de formaldehído con alkyl cianoacrilato, obteniéndose así un prepolímero, el cual por calentamiento es despolimerizado en un líquido monómero. Dicho monómero puede ser modificado para obtener distintos compuestos de longitudes de cadena diferentes. Algunos pegamentos son 100% etil cianoacrilato y otros tienen una mezcla en su composición. En la aplicación sobre tejidos vivos, el monómero sufre una reacción de hidroxilación exotérmica que resulta en una polimerización del adhesivo.
Aplicaciones Médicas del Cianoacrilato
Los primeros usos médicos del cianoacrilato lo fueron en soldados americanos durante la guerra de Vietnam en los años 60, empleado como sutura y como agente hemostático, para heridas con sangrado imparable (ejemplo: heridas de pecho). Se administraba en spray y resultaba muy efectivo para parar el sangrado.
El pegamento de cianoacrilato del comercio no es apto para uso médico, pues está hecho de una cadena corta de cianoacrilato (metil cianoacrilato o etil cianoacrilato), que no es compatible con el tejido humano, debido a que se degradan rápidamente y dan productos tóxicos que podrían empeorar la herida. Para uso médico se emplean cianoacrilatos de cadena larga y el tipo de adhesivo depende de la parte del cuerpo donde se aplique.
En los años 1980 surgió la idea de distribuir medicinas a lugares específicos del cuerpo mediante nanoesferas o nanopartículas, que podrían contener drogas de liberación prolongada en el cuerpo. Estas esferas de cianoacrilato de cadena larga estarían rellenas de una droga activa o adsorbida en su superficie. De este modo se podrían distribuir péptidos, proteínas, vacunas o antiproteasas, administradas oral o intravenosamente. Esto tiene especial interés en el caso de los tumores, pues la droga causa efectos secundarios y solo debería llegar al tumor.
Toxicidad y Efectos Secundarios del Cianoacrilato
El calentamiento del metil cianoacrilato causa despolimerización produciendo productos gaseosos fuertemente irritantes para los pulmones y los ojos. Los derivados del cianoacrilato de cadena más corta tienen más grado de toxicidad para los tejidos que los de cadena larga.
Inyectado subcutáneamente el cianoacrilato produce inflamación, necrosis tisular y granulación, al causar toxicidad histológica debido a los productos de degradación como el formaldehído. Los componentes de cadena larga se degradan más lentamente produciéndose menos toxicidad al liberar esos productos más gradualmente.
Es aconsejado no usar en mucosa oral, manos, pies o en articulaciones, donde los movimientos repetitivos y el lavado pudieran causar la pérdida prematura del adhesivo. Tampoco se debería usar en heridas de úlceras de decúbito, y en mordidas humana o animal.
Situada sobre la herida actúa como una barrera para la epitelización, sin embargo también puede causar reacciones de cuerpo extraño e incrementar el riesgo de infección. Cuando el cianoacrilato es colocado profundamente en alvéolos postextracción o bajo colgajos puede provocar reacciones de cuerpo extraño.
Para evitar la toxicidad, en odontología se han desarrollado diferentes formas de cianoacrilato como metil, etil, isobutil, isohexil y octil. El n-butil-2-cianoacrilato es comúnmente usado para cerrar heridas a baja tensión, aunque sus efectos sobre hígado y riñón no son conocidos. Hay descrita la aparición de leucemia linfoblástica aguda en un paciente con exposición crónica de la mucosa oral a cianoacrilato.
¿Qué Hacer Ante Problemas Dentales Comunes?
Si tienes una corona sobre un diente natural y, por algún motivo, se cae, lo ideal es que sea un dentista quien vuelva a cementarla. Morder con excesiva fuerza, rechinar los dientes o no colocar adecuadamente la prótesis puede hacer que termine rompiéndose.
Recibir un fuerte golpe en la boca acarrea graves consecuencias para la salud oral, siendo una de las más visibles los dientes rotos. Si sucede, debemos acudir con celeridad a nuestra dentista de confianza, pero nunca recurrir a adhesivos para intentar reparar la pieza y mucho menos emplear otros productos de índole industrial. Fruto también de un traumatismo en la dentadura es el aflojamiento de una pieza, sin que esta llegue a caerse. Este tipo de urgencias dentales es más habitual en niños, pero puede suceder a cualquier edad.
¡Importante! Nunca intentes pegar un diente suelto por un golpe con pegamento Super Glue ni nada similar, podrías arruinar las posibilidades de salvarlo.
En caso de diente astillado o grieta, tampoco apliques nada por tu cuenta. Mantén la higiene, quizás cubre la parte filosa con cera dental (como la ortodóntica, si te está irritando) y acude a consulta.
Conclusión
Los pegamentos dentales pueden ser útiles para asegurar las prótesis removibles, pero es crucial utilizarlos correctamente y ser conscientes de los posibles efectos secundarios. Consultar a un profesional dental es esencial para abordar cualquier problema y asegurar una salud oral óptima.
tags: #efectos #secundarios #de #los #pegamentos #dentales